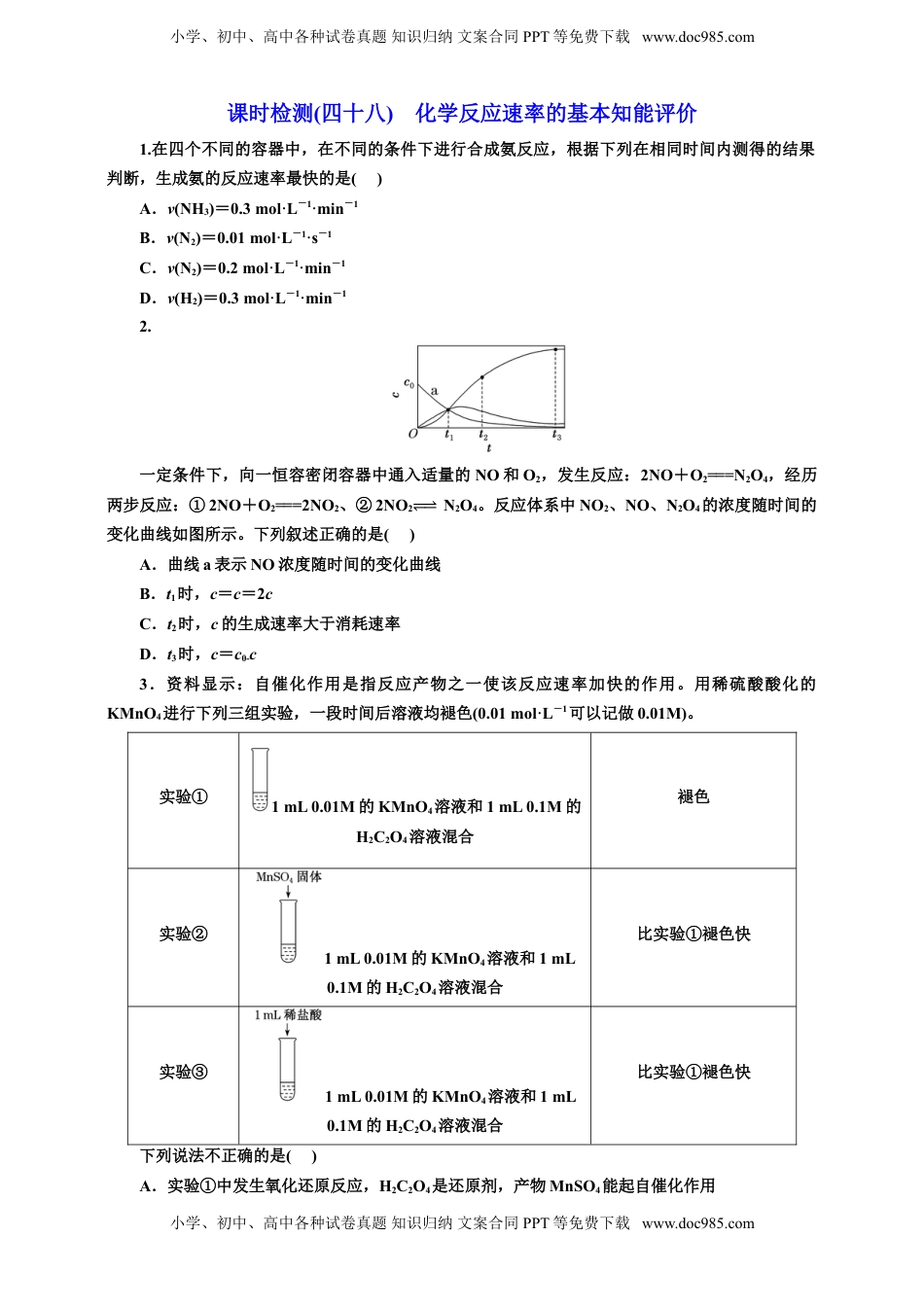
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com课时检测(四十八)化学反应速率的基本知能评价1.在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是()A.v(NH3)=0.3mol·L-1·min-1B.v(N2)=0.01mol·L-1·s-1C.v(N2)=0.2mol·L-1·min-1D.v(H2)=0.3mol·L-1·min-12.一定条件下,向一恒容密闭容器中通入适量的NO和O2,发生反应:2NO+O2===N2O4,经历两步反应:①2NO+O2===2NO2、②2NO2⥫⥬N2O4。反应体系中NO2、NO、N2O4的浓度随时间的变化曲线如图所示。下列叙述正确的是()A.曲线a表示NO浓度随时间的变化曲线B.t1时,c=c=2cC.t2时,c的生成速率大于消耗速率D.t3时,c=c0-c3.资料显示:自催化作用是指反应产物之一使该反应速率加快的作用。用稀硫酸酸化的KMnO4进行下列三组实验,一段时间后溶液均褪色(0.01mol·L-1可以记做0.01M)。实验①1mL0.01M的KMnO4溶液和1mL0.1M的H2C2O4溶液混合褪色实验②1mL0.01M的KMnO4溶液和1mL0.1M的H2C2O4溶液混合比实验①褪色快实验③1mL0.01M的KMnO4溶液和1mL0.1M的H2C2O4溶液混合比实验①褪色快下列说法不正确的是()A.实验①中发生氧化还原反应,H2C2O4是还原剂,产物MnSO4能起自催化作用小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comB.实验②褪色比①快,是因为MnSO4的催化作用加快了反应速率C.实验③褪色比①快,是因为Cl-的催化作用加快了反应速率D.若用1mL0.2M的H2C2O4做实验①,推测比实验①褪色快4.(2022·广东等级考)在相同条件下研究催化剂Ⅰ、Ⅱ对反应X―→2Y的影响,各物质浓度c随反应时间t的部分变化曲线如图,则()A.无催化剂时,反应不能进行B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化D.使用催化剂Ⅰ时,0~2min内,v(X)=1.0mol·L-1·min-15.(2024·全国高三专题练习)2SO2(g)+O2(g)⥫⥬2SO3(g)ΔH=-198kJ·mol-1,在V2O5存在时,该反应的机理为V2O5+SO2===2VO2+SO3(快),4VO2+O2===2V2O5(慢)。下列说法正确的是()A.反应速率主要取决于V2O5的质量B.VO2是该反应的催化剂C.逆反应的活化能大于198kJ·mol-1D.增大SO2的浓度可显著提高反应速率6.为了探究温度、硫酸铜对锌与稀硫酸反应生成氢气速率的影响,某同学设计了如下方案:编号纯锌粉质量0.2mol·L-1稀硫酸体积温度硫酸铜固体质量Ⅰ2.0g10.0mL25℃0Ⅱ2.0g10.0mLt℃0Ⅲ2.0g10.0mL35℃0.2gⅣ2.0g10.0mL35℃4.0g下列推断合理的是()A.选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,必须控制t=25B.待测物理量是收集等体积(相同条件)的气体所需要的时间,时间越长,反应越快C.根据该方案,还可以探究稀硫酸浓度对反应速率的影响D.根据该实验方案得出反应速率的大小可能是Ⅲ>Ⅱ>Ⅰ>Ⅳ7.工业废水中的有机物能够引起水体污染,导致水体富营养化。其中Fenton法常用于处理含难降解有机物的工业废水,往调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物pCP,控制pCP的初始浓度相同,恒定实验温度在小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com298K或313K进行实验。实验测得pCP的浓度随时间变化的关系如图所示,下列说法不正确的是()A.由①可得,降解反应在50~150s内的反应速率:v(pCP)=8.0×10-6mol·L-1·s-1B.升高温度,有利于加快降解反应速率,所以温度越高越有利于降解C.③目的为探究溶液的pH对降解反应速率的影响D.298K下,pH=10时有机物pCP降解速率比pH=3时慢8.(2024·襄阳模拟)某化学小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们完成一些判断。将5.4g铝片投入500mL0.5mol·L-1的硫酸溶液中,如图为反应产生氢气速率与反应时间的关系图。(1)关于图像的描述不正确的是_______...






















发表评论取消回复