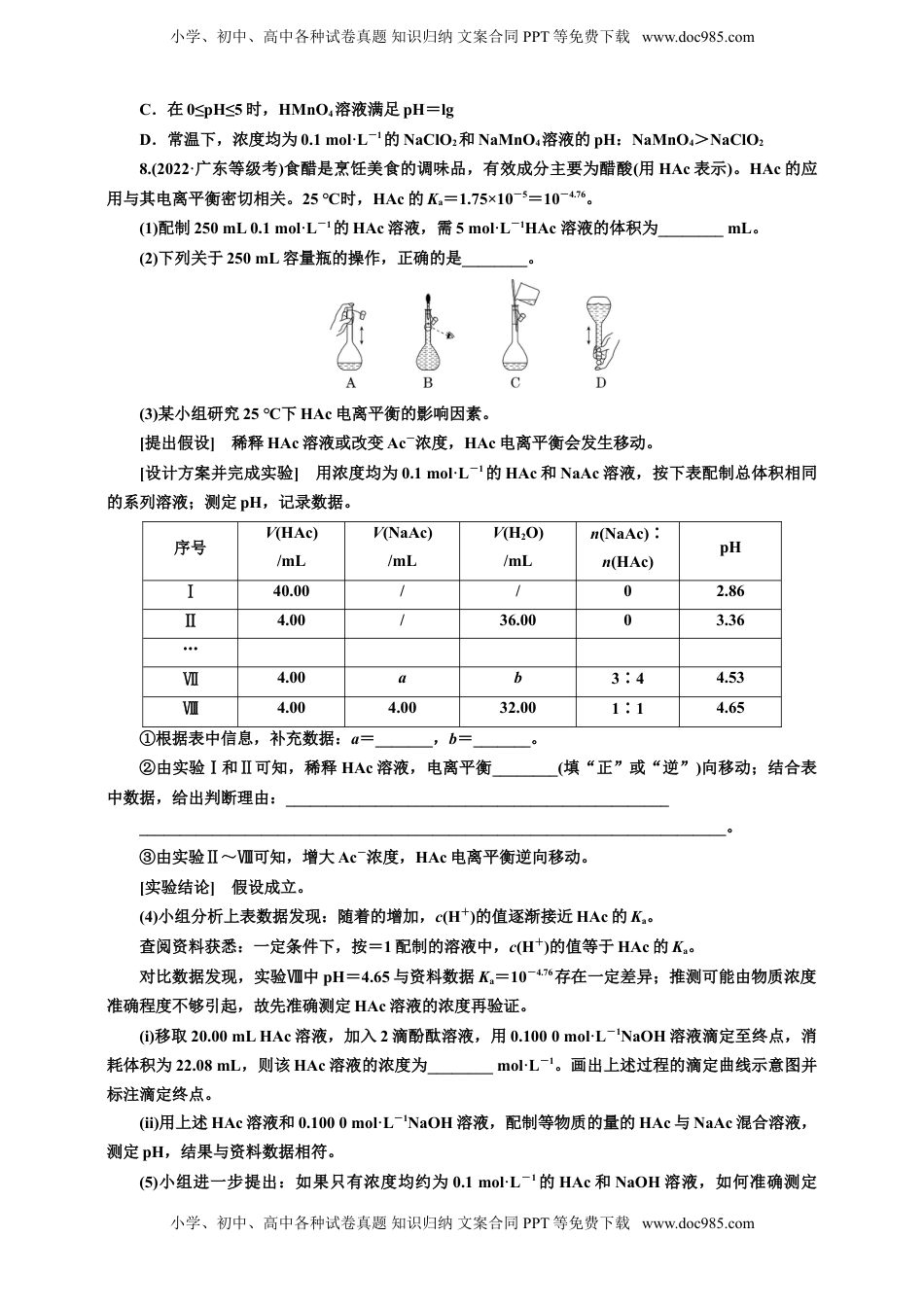
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com课时检测(五十七)pH计算与酸碱中和滴定的拓展应用1.在室温下,等体积的酸和碱的溶液混合后,pH一定小于7的是()A.pH=3的HNO3和pH=11的KOH溶液B.pH=3的盐酸和pH=11的氨水C.pH=3的醋酸和pH=11的Ba(OH)2溶液D.pH=3的硫酸和pH=11的NaOH溶液2.(2023·重庆等级考)(NH4)2SO4溶解度随温度变化的曲线如图所示,关于各点对应的溶液,下列说法正确的是()A.M点Kw等于N点KwB.M点pH大于N点pHC.N点降温过程中有2个平衡发生移动D.P点c(H+)+c(NH)+c(NH3·H2O)=c(OH-)+2c(SO)3.(2024·福建福州模拟)下列滴定中,指示剂的选择或滴定终点颜色变化有错误的是()提示:2KMnO4+5K2SO3+3H2SO4===6K2SO4+2MnSO4+3H2O、I2+Na2S===2NaI+S↓选项滴定管中的溶液锥形瓶中的溶液指示剂滴定终点颜色变化ANaOH溶液CH3COOH溶液酚酞无色→浅红色BHCl溶液氨水酚酞浅红色→无色C酸性KMnO4溶液K2SO3溶液无无色→浅紫红色D碘水Na2S溶液淀粉无色→蓝色4.生产和实验中广泛采用甲醛法测定饱和食盐水样品中的NH含量,利用的反应原理为4NH+6HCHO===(CH2)6N4H+(一元酸)+3H++6H2O。实验步骤如下:①甲醛中常含有微量甲酸,应先除去。取甲醛amL于锥形瓶,加入1~2滴指示剂,用浓度为bmol·L-1的NaOH溶液滴定,滴定管的初始读数为V1mL,当锥形瓶内溶液呈微红色时,滴定管的读数为V2mL。②向锥形瓶中加入饱和食盐水试样cmL,静置1分钟。③用上述滴定管中剩余的NaOH溶液继续滴定锥形瓶内溶液,至溶液呈微红色时,滴定管的读数为V3mL。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com下列说法不正确的是()A.步骤①中的指示剂可以选用酚酞溶液B.步骤②中静置的目的是使NH和HCHO完全反应C.步骤②若不静置会导致测定结果偏高D.饱和食盐水中的c(NH)=mol·L-15.中和滴定是一种操作简单,准确度高的定量分析方法,实际工作中也可利用物质间的氧化还原反应、沉淀反应进行类似的滴定分析。这些滴定分析均需要通过指示剂来确定滴定终点,下列对几种具体的滴定分析(待测液置于锥形瓶内)中所用指示剂及滴定终点时的溶液颜色的判断不正确的是()A.利用“H++OH-===H2O”原理来测量某氢氧化钠溶液的浓度时:甲基橙——橙色B.利用“2Fe3++2I-===I2+2Fe2+”原理,用NaI溶液测量Fe(NO3)3样品中Fe(NO3)3百分含量:淀粉——蓝色C.利用“Ag++SCN-===AgSCN↓”原理,可用标准KSCN溶液测AgNO3溶液浓度:Fe(NO3)3——血红色D.用标准酸性KMnO4溶液滴定NaHSO3溶液以测量其浓度:KMnO4——紫红色6.实验室常用准确称量的邻苯二甲酸氢钾(,溶液呈弱酸性)来测定配制的NaOH标准溶液的浓度,即分析化学实验中常称为“标定”的一种方法。某学生将配好的待测NaOH溶液放于锥形瓶中,用该溶液标定,进行了四次实验,数据如表:实验编号1234消耗标准液V()18.6017.1016.9017.00下列说法正确的是()A.实验中最好选择酚酞作指示剂B.滴定过程中消耗的V平均(邻苯二甲酸氢钾)=17.40mLC.配制邻苯二甲酸氢钾溶液时,容量瓶洗净后未经干燥处理,会使最终标定结果偏高D.锥形瓶在装液前未用待测NaOH溶液润洗会使标定结果偏低7.常温时,1mol·L-1HClO2和1mol·L-1HMnO4两种酸溶液,起始时的体积均为V0,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是()A.稀释前分别用1mol·L-1的NaOH溶液中和,消耗的NaOH溶液体积:HMnO4>HClO2B.当稀释至pH均为3时,溶液中c(ClO)>c(MnO)小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comC.在0≤pH≤5时,HMnO4溶液满足pH=lgD.常温下,浓度均为0.1mol·L-1的NaClO2和NaMnO4溶液的pH:NaMnO4>NaClO28.(2022·广东等级考)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离平衡密切相关。25℃时,HAc的Ka=1.75×10-5=10-4.76。...






















发表评论取消回复