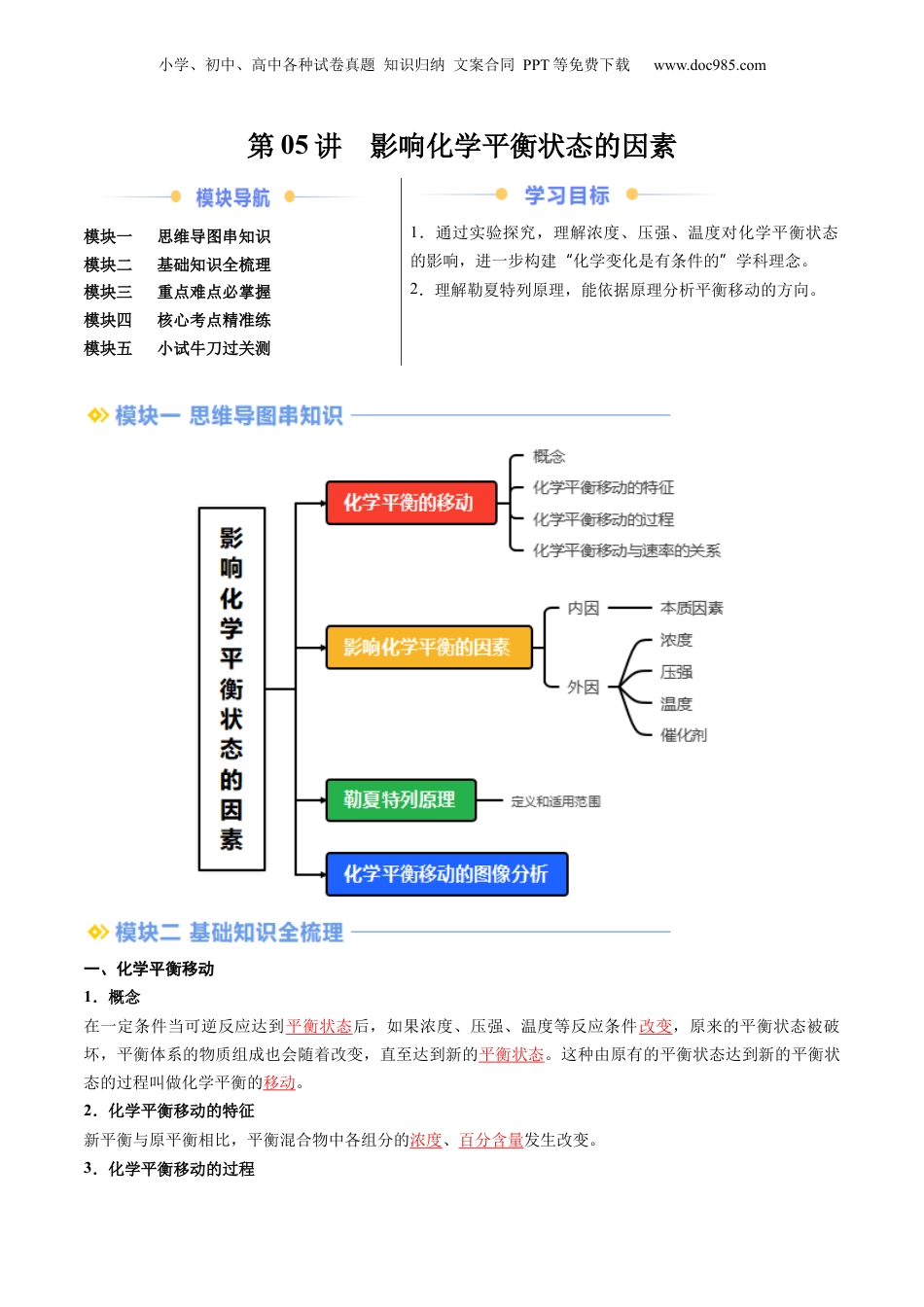
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com第05讲影响化学平衡状态的因素模块一思维导图串知识模块二基础知识全梳理模块三重点难点必掌握模块四核心考点精准练模块五小试牛刀过关测1.通过实验探究,理解浓度、压强、温度对化学平衡状态的影响,进一步构建化学变化是有条件的学科理念。“”2.理解勒夏特列原理,能依据原理分析平衡移动的方向。一、化学平衡移动1.概念在一定条件当可逆反应达到平衡状态后,如果浓度、压强、温度等反应条件改变,原来的平衡状态被破坏,平衡体系的物质组成也会随着改变,直至达到新的平衡状态。这种由原有的平衡状态达到新的平衡状态的过程叫做化学平衡的移动。2.化学平衡移动的特征新平衡与原平衡相比,平衡混合物中各组分的浓度、百分含量发生改变。3.化学平衡移动的过程小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com4.化学平衡移动与化学反应速率的关系①v正>v逆:平衡向正反应方向移动。②v正=v逆:反应达到平衡状态,平衡不发生移动。③v正<v逆:平衡向逆反应方向移动。二、影响化学平衡的因素浓度对化学平衡的影响实验原理Fe3++3SCN-Fe(SCN)3实验操作现象与结论b溶液颜色变浅,平衡向逆反应方向移动c溶液颜色变深,平衡向正反应方向移动1.浓度对化学平衡的影响(1)规律当其他条件不变时:增大反应物浓度或减小生成物浓度,平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,平衡向逆反应方向移动。(2)解释①增大反应物浓度或减小生成物浓度,Q减小,则Q<K,平衡向正反应方向移动。减小反应物浓度或增大生成物浓度,②Q增大,则Q>K,平衡向逆反应方向移动。压强对化学平衡的影响实验原理2NO2N2O4实验步骤活塞处处,压强Ⅱ→Ⅰ增大活塞处处,压强减小Ⅰ→Ⅱ实验现象混合气体的颜色先变深又逐渐变浅混合气体的颜色先变浅又逐渐变深实验结论活塞往里推,体积减小,压强增大,c(NO2)增大,颜色变深,但颜色又变浅,说明c(NO2)减小,平衡向正反应方向移动。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com活塞往外拉,体积增大,压强减小,c(NO2)减小,颜色变浅,但气体颜色又变深,说明c(NO2)增大,平衡向逆反应方向移动2.压强对化学平衡的影响(1)规律对于有气体参加的可逆反应,在其他条件不变时:反应前后气体体积改变增大压强向气体分子总数减小的方向移动减小压强向气体分子总数增大的方向移动反应前后气体体积不变改变压强平衡不移动(2)解释化学方程式中气态物质系数的变化压强变化Q值变化Q与K的关系平衡移动方向增大增大增大Q>K逆向移动减小减小Q<K正向移动减小增大减小Q<K正向移动减小增大Q>K逆向移动不变增大不变Q=K不移动减小压强的影响实质是浓度的影响,所以只有当这些改变造成浓度改变时,平衡才有可能移动。如惰性“”“气体对化学平衡的影响:”恒温恒容原平衡体系―———―→体系总压强增大―体系中各组分的浓度不变→―平衡不移动→恒温恒压原平衡体系―———―→容器容积增大,各反应气体的分压减小―反应气体的浓度同倍数减小→(等效于减压)——压强对化学平衡的影响实验原理2NO2N2O4ΔH=-56.9kJ·mol-1实验步骤实验现象热水中混合气体颜色加深;冰水中混合气体颜色变浅实验结论混合气体受热颜色加深,说明NO2浓度增大,即平衡向逆反应方向移动;混合气体被冷却时颜色变浅,说明NO2浓度减小,即平衡向正反应方向移动3.温度对化学平衡的影响(1)规律小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com当其他条件不变时:升高温度,平衡向吸热反应方向移动;降低温度,平衡向放热反应方向移动。(2)解释用v—t图像分析反应:mA(g)+nB(g)pC(g)ΔH<0。t1时刻,升高温度,v′正、v′逆均增大,但吸热反应方向的v′逆增大幅度大,则v′逆>v′正,平衡逆向移动t1时刻,降低温度,v′正、v′逆均减小,但吸热反应方向的v′逆减小幅度大。则v′正>v′逆,平衡正向移动4.催化剂对化学平衡的影响(1)规律当其他条件不变时:催化剂不能改变达到化学平衡状态时反应混合物的组...




















发表评论取消回复