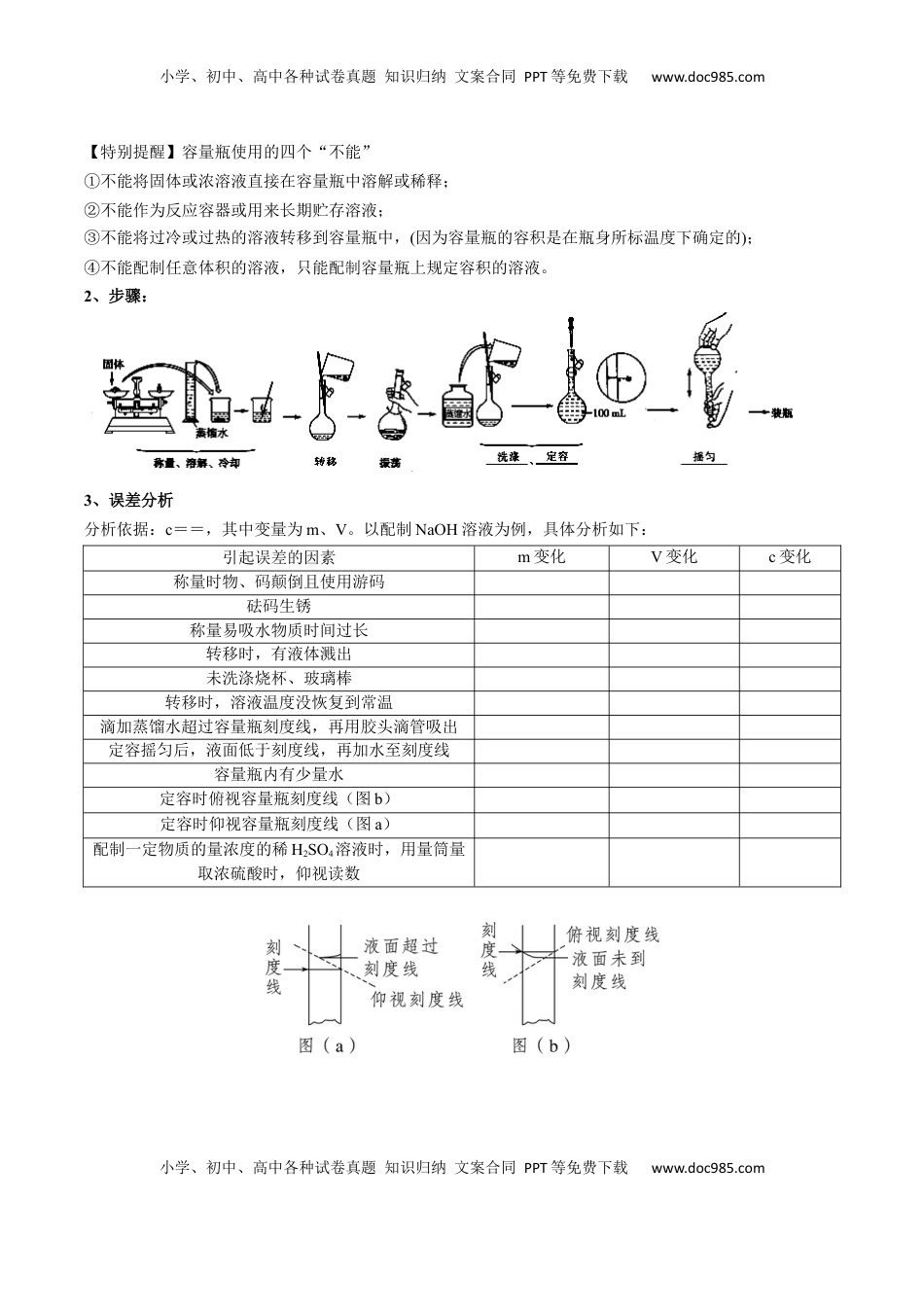
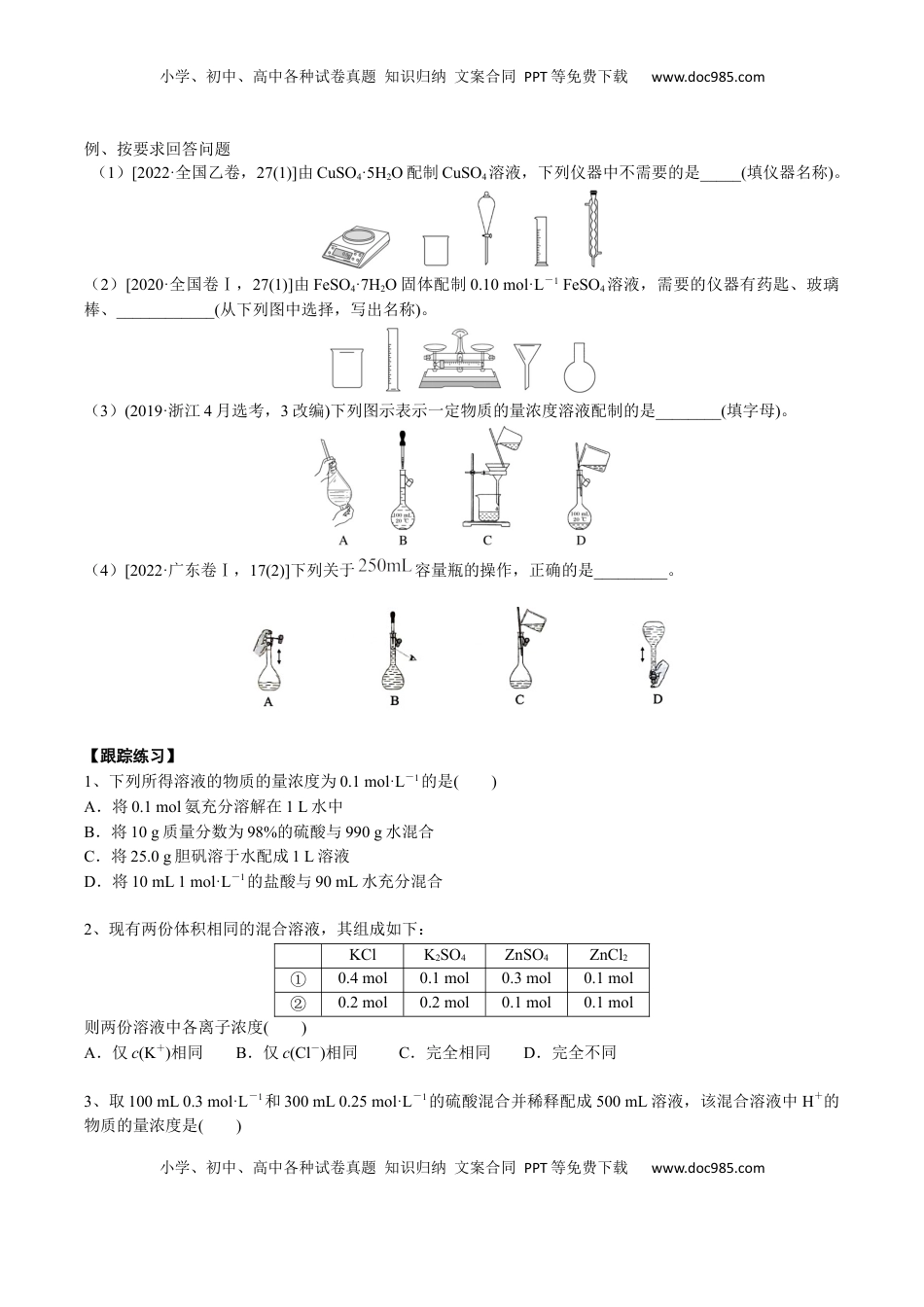
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【基础知识】物质的量及计算考点三物质的量在化学实验中的应用【必备知识】一、物质的量浓度及其计算1、物质的量浓度(1)概念物质的量浓度表示单位体积的溶液里所含溶质B的物质的量,也称为B的物质的量浓度,符号为cB。(2)表达式:cB=。(3)常用单位:或mol·m-3,有时也用mmol·L-1。(4)特点:对于某浓度的溶液,取出任意体积的溶液,其浓度、密度、质量分数均不变,但所含溶质的质量、物质的量因体积不同而改变。(5)与质量分数ω的换算公式:。2、溶液稀释定律(守恒观点)(1)溶质的质量在稀释前后保持不变,即ω稀m稀=ω浓m浓。(2)溶质的物质的量在稀释前后保持不变,即。(3)溶液质量守恒(体积一般不守恒)。3、同溶质不同物质的量浓度溶液的混合计算(1)混合后溶液体积保持不变时,c1V1+c2V2=c混×(V1+V2)。(2)混合后溶液体积发生改变时,c1V1+c2V2=c混V混,其中V混=。例、按要求回答问题(1)在标准状况下,将VL氨气溶于0.1L水中,所得溶液的密度为ρg·cm-3,则此氨水的物质的量浓度为________mol·L-1。(2)将25gCuSO4·5H2O晶体溶于75g水中,配成溶液,所得溶液的溶质质量分数为________。(3)将amL5mol·L-1NaCl溶液稀释至bmL,稀释后溶液中Cl-的物质的量浓度为________。(4)200mL0.3mol·L-1K2SO4溶液和100mL0.2mol·L-1Fe2(SO4)3溶液混合后不考虑混合后溶液体积的变化,溶液中SO的物质的量浓度为________。二、溶液的配制1、仪器:玻璃棒、容量瓶、胶头滴管、烧杯、天平、量筒。(1)托盘天平:①物码②精确度g(2)容量瓶:检漏操作:小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【特别提醒】容量瓶使用的四个“不能”①不能将固体或浓溶液直接在容量瓶中溶解或稀释;②不能作为反应容器或用来长期贮存溶液;③不能将过冷或过热的溶液转移到容量瓶中,(因为容量瓶的容积是在瓶身所标温度下确定的);④不能配制任意体积的溶液,只能配制容量瓶上规定容积的溶液。2、步骤:3、误差分析分析依据:c==,其中变量为m、V。以配制NaOH溶液为例,具体分析如下:引起误差的因素m变化V变化c变化称量时物、码颠倒且使用游码砝码生锈称量易吸水物质时间过长转移时,有液体溅出未洗涤烧杯、玻璃棒转移时,溶液温度没恢复到常温滴加蒸馏水超过容量瓶刻度线,再用胶头滴管吸出定容摇匀后,液面低于刻度线,再加水至刻度线容量瓶内有少量水定容时俯视容量瓶刻度线(图b)定容时仰视容量瓶刻度线(图a)配制一定物质的量浓度的稀H2SO4溶液时,用量筒量取浓硫酸时,仰视读数小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com例、按要求回答问题(1)[2022·全国乙卷,27(1)]由CuSO4·5H2O配制CuSO4溶液,下列仪器中不需要的是_____(填仪器名称)。(2)[2020·全国卷Ⅰ,27(1)]由FeSO4·7H2O固体配制0.10mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、____________(从下列图中选择,写出名称)。(3)(2019·浙江4月选考,3改编)下列图示表示一定物质的量浓度溶液配制的是________(填字母)。(4)[2022·广东卷Ⅰ,17(2)]下列关于容量瓶的操作,正确的是_________。【跟踪练习】1、下列所得溶液的物质的量浓度为0.1mol·L-1的是()A.将0.1mol氨充分溶解在1L水中B.将10g质量分数为98%的硫酸与990g水混合C.将25.0g胆矾溶于水配成1L溶液D.将10mL1mol·L-1的盐酸与90mL水充分混合2、现有两份体积相同的混合溶液,其组成如下:KClK2SO4ZnSO4ZnCl2①0.4mol0.1mol0.3mol0.1mol②0.2mol0.2mol0.1mol0.1mol则两份溶液中各离子浓度()A.仅c(K+)相同B.仅c(Cl-)相同C.完全相同D.完全不同3、取100mL0.3mol·L-1和300mL0.25mol·L-1的硫酸混合并稀释配成500mL溶液,该混合溶液中H+的物质的量浓度是()小学、初中...