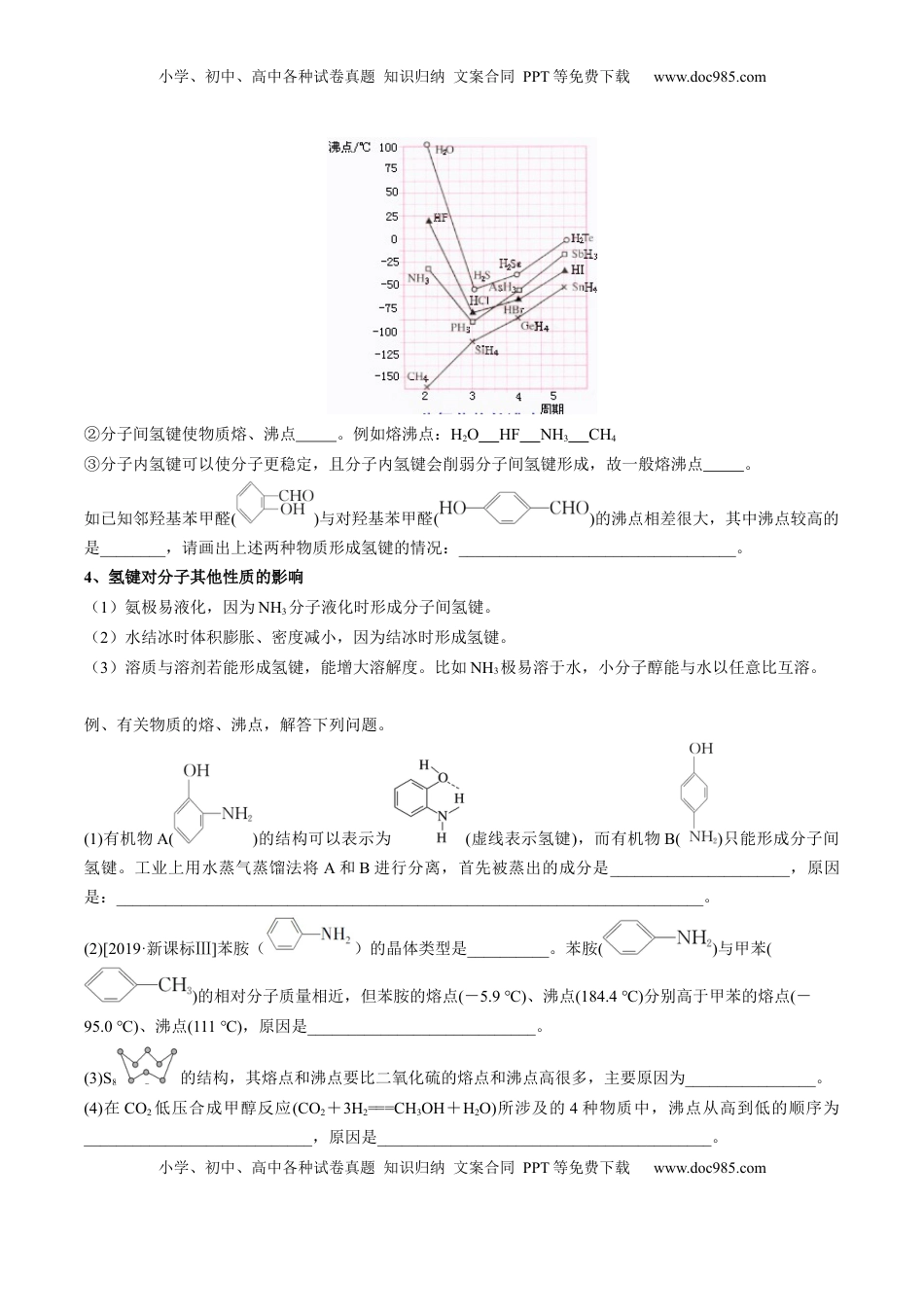
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【基础知识】分子结构与性质考点七分子间作用力【必备知识】1、范德华力、氢键的对比范德华力氢键作用微粒分子或原子(稀有气体分子)H与N、O、F等电负性很大的原子分类分子内氢键和分子间氢键特征方向性和饱和性饱和性和方向性强度化学键氢键范德华力影响其强度的因素①组成和结构相似的物质,相对分子质量,范德华力越大;②分子的极性,范德华力越大。X—H…Y强弱与X和Y的电负性有关。电负性越,氢键越强。对物质性质的影响主要影响物理性质(如熔、沸点)2、氢键的表示方法(以HF分子间氢键为例)3、分子间作用力对物质溶沸点的影响①一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力,物质的熔沸点越高。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com②分子间氢键使物质熔、沸点。例如熔沸点:H2OHFNH3CH4③分子内氢键可以使分子更稳定,且分子内氢键会削弱分子间氢键形成,故一般熔沸点。如已知邻羟基苯甲醛()与对羟基苯甲醛()的沸点相差很大,其中沸点较高的是________,请画出上述两种物质形成氢键的情况:__________________________________。4、氢键对分子其他性质的影响(1)氨极易液化,因为NH3分子液化时形成分子间氢键。(2)水结冰时体积膨胀、密度减小,因为结冰时形成氢键。(3)溶质与溶剂若能形成氢键,能增大溶解度。比如NH3极易溶于水,小分子醇能与水以任意比互溶。例、有关物质的熔、沸点,解答下列问题。(1)有机物A()的结构可以表示为(虚线表示氢键),而有机物B()只能形成分子间氢键。工业上用水蒸气蒸馏法将A和B进行分离,首先被蒸出的成分是______________________,原因是:________________________________________________________________________。(2)[2019·新课标Ⅲ]苯胺()的晶体类型是__________。苯胺()与甲苯()的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(111℃),原因是____________________________。(3)S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为________________。(4)在CO2低压合成甲醇反应(CO2+3H2===CH3OH+H2O)所涉及的4种物质中,沸点从高到低的顺序为____________________________,原因是_________________________________________。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【易错辨析】1、氢键是一种特殊的化学键()2、卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大()3、氨水中氨分子与水分子间形成了氢键()4、可燃冰(CH4·8H2O)中甲烷分子与水分子之间形成了氢键()5、H2O比H2S稳定是因为水分子间存在氢键()6、氢键的存在一定能使物质的熔、沸点升高()7、NH3的稳定性很强,是因为其分子间能形成氢键。()8、C的氢化物沸点低于O的氢化物,因为H2O含有氢键。()9、范德华力非常微弱,破坏范德华力不需要消耗能量。()10、H2O2分子间存在氢键。()11、氢键具有方向性和饱和性。()12、乙醇分子和水分子间只存在范德华力。()【跟踪练习】1、下列物质能形成氢键,且形成的氢键最强的是()A、甲醇B、NH3C、冰D、(HF)n2、氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,根据氨水的性质可推知NH3·H2O的结构式为()3、下列关于化学键及晶体的说法中,不正确的是()A.Cl2、Br2、I2的沸点逐渐升高,是因为分子间作用力越来越大B.NaOH和NH4Cl化学键类型相同C.N2和CCl4两种分子中,每个原子的最外层都具有8电子稳定结构D.石英晶体是共价晶体,其分子式为SiO24、下列现象与氢键有关的是()HF①的熔、沸点比ⅦA族其他元素氢化物的高②乙醇可以和水以任意比互溶③冰的密度比液态水的密度小④水分子高温下也很稳...