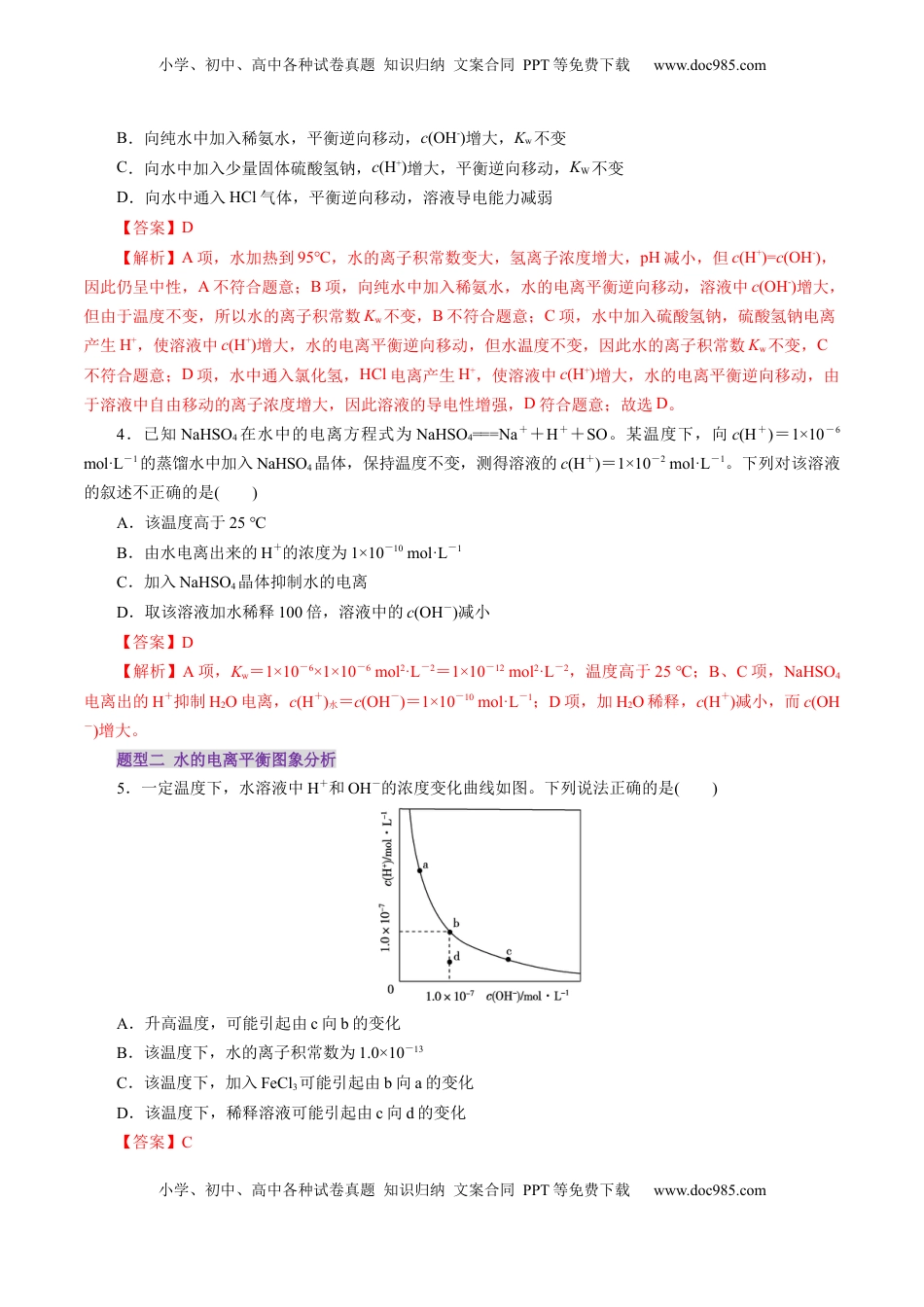
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com第02讲水的电离和溶液的酸碱性目录01模拟基础练【题型一】水的电离平衡及影响因素【题型二】水的电离平衡图象分析【题型三】溶液的酸碱性与pH【题型四】酸碱中和滴定操作及误差分析【题型五】酸碱中和滴定图像【题型六】酸碱中和滴定拓展02重难创新练03真题实战练题型一水的电离平衡及影响因素1.下列条件变化会使H2O的电离平衡向电离方向移动,且pH<7的是()A.将纯水加热到100℃B.向水中加少量HClC.向水中加入少量NaOHD.向水中加少量Na2CO3【答案】A【解析】A项,H2O的电离是吸热反应,加热,促进水的电离,pH<7,A正确;B项,向水中加入HCl,抑制水的电离,pH<7,B错误;C项,向水中加入NaOH,抑制水的电离,pH>7,C错误;D项,向水中加入Na2CO3,促进水的电离,pH>7,D错误。2.一定温度下,水存在H2OH++OH-ΔH=Q(Q>0)的平衡,下列叙述一定正确的是()A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小B.将水加热,Kw增大,pH减小C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低D.向水中加入少量固体硫酸钠,c(H+)=10-7mol·L-1,Kw不变【答案】B【解析】A项,Kw只与温度有关;B项正确;C项,加入CH3COONa,促进水的电离,溶液呈碱性;D项,该题没有指明是常温下,所以c(H+)不一定等于10-7mol·L-1。3.25°C时,水的电离达到平衡:H2OH++OH-,下列叙述不正确的是()A.将纯水加热到95℃时,Kw变大,pH减小,水仍呈中性小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comB.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw不变C.向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,KW不变D.向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱【答案】D【解析】A项,水加热到95℃,水的离子积常数变大,氢离子浓度增大,pH减小,但c(H+)=c(OH-),因此仍呈中性,A不符合题意;B项,向纯水中加入稀氨水,水的电离平衡逆向移动,溶液中c(OH-)增大,但由于温度不变,所以水的离子积常数Kw不变,B不符合题意;C项,水中加入硫酸氢钠,硫酸氢钠电离产生H+,使溶液中c(H+)增大,水的电离平衡逆向移动,但水温度不变,因此水的离子积常数Kw不变,C不符合题意;D项,水中通入氯化氢,HCl电离产生H+,使溶液中c(H+)增大,水的电离平衡逆向移动,由于溶液中自由移动的离子浓度增大,因此溶液的导电性增强,D符合题意;故选D。4.已知NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO。某温度下,向c(H+)=1×10-6mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2mol·L-1。下列对该溶液的叙述不正确的是()A.该温度高于25℃B.由水电离出来的H+的浓度为1×10-10mol·L-1C.加入NaHSO4晶体抑制水的电离D.取该溶液加水稀释100倍,溶液中的c(OH-)减小【答案】D【解析】A项,Kw=1×10-6×1×10-6mol2·L-2=1×10-12mol2·L-2,温度高于25℃;B、C项,NaHSO4电离出的H+抑制H2O电离,c(H+)水=c(OH-)=1×10-10mol·L-1;D项,加H2O稀释,c(H+)减小,而c(OH-)增大。题型二水的电离平衡图象分析5.一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是()A.升高温度,可能引起由c向b的变化B.该温度下,水的离子积常数为1.0×10-13C.该温度下,加入FeCl3可能引起由b向a的变化D.该温度下,稀释溶液可能引起由c向d的变化【答案】C小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【解析】A.c点溶液中c(OH-)>c(H+),溶液呈碱性,升温,溶液中c(OH-)不可能减小。B.由b点对应c(H+)与c(OH-)可知,Kw=c(H+)·c(OH-)=1.0×10-7×1.0×10-7=1.0×10-14。C.FeCl3溶液水解显酸性,溶液中c(H+)增大,因一定温度下水的...