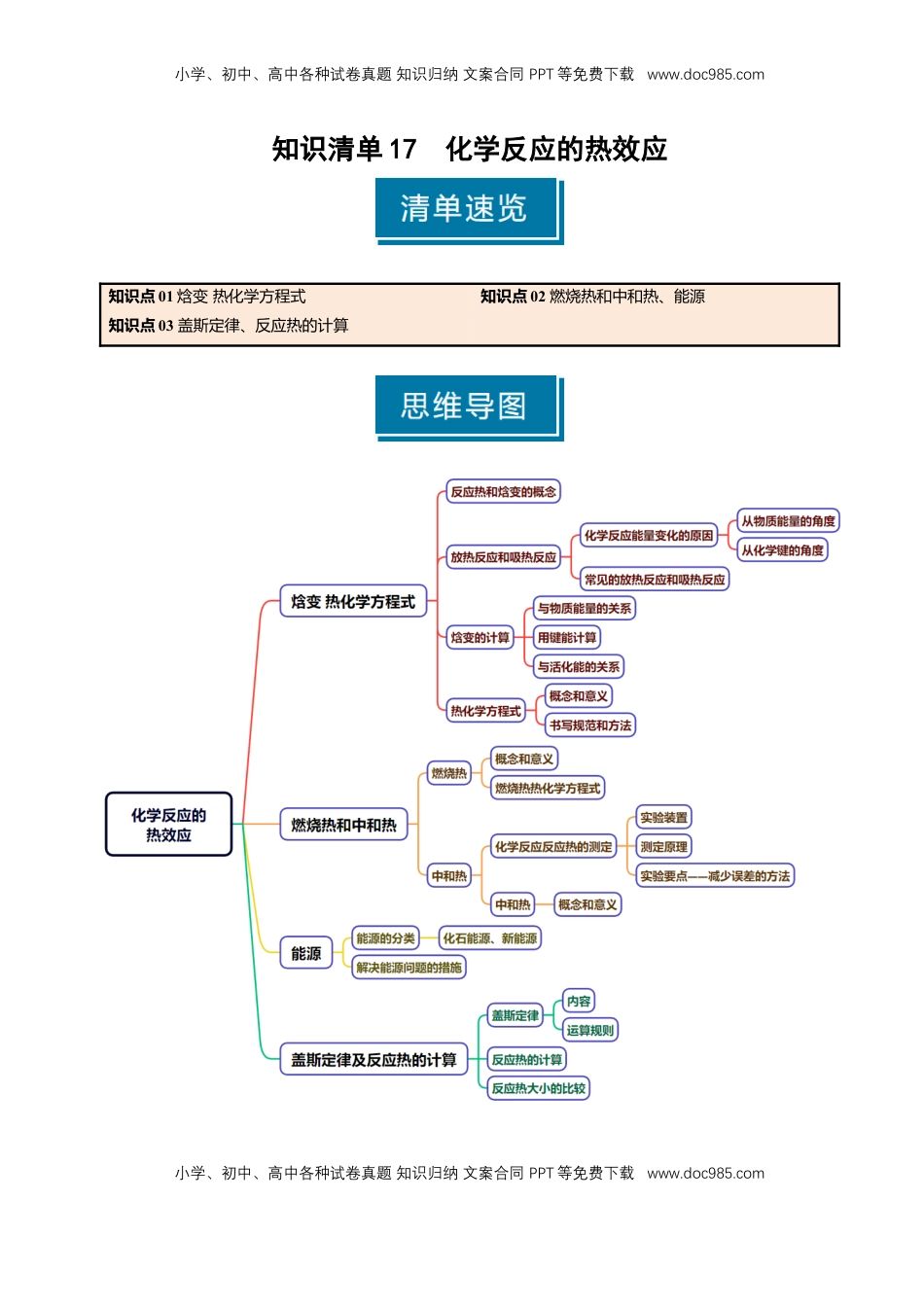
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com知识清单17化学反应的热效应知识点01焓变热化学方程式知识点02燃烧热和中和热、能源知识点03盖斯定律、反应热的计算小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com知识点01焓变热化学方程式1.反应热和焓变(1)反应热:化学反应过程中_______或_______的能量。(2)焓变:恒压条件下的反应热,称之为焓变,符号为_______,单位为____________。2.放热反应和吸热反应(1)化学反应放热和吸热的原因判断依据放热反应吸热反应反应物总能量与生成物总能量的相对大小反应物具有的总能量_______生成物具有的总能量反应物具有的总能量_______生成物具有的总能量与化学键的关系生成物分子成键时释放出的总能量_______反应物分子断键时吸收的总能量生成物分子成键时释放出的总能量_______反应物分子断键时吸收的总能量ΔH的符号ΔH<0(“-”号)ΔH>0(“+”号)反应过程图示(2)常见的放热反应和吸热反应放热反应吸热反应常见反应①可燃物的燃烧②酸碱中和反应③金属与酸的置换反应④物质的缓慢氧化⑤铝热反应⑥大多数化合反应①弱电解质的电离②盐类的水解反应③Ba(OH)2·8H2O与NH4Cl的反应④C和H2O(g)、C和CO2的反应⑤大多数分解反应3.反应焓变的计算(1)计算方法小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comΔH=_______的总能量-_______的总能量ΔH=_______的总键能-_______的总键能ΔH=_______活化能-_______活化能(2)用键能计算反应热利用键能计算反应热的关键,是弄清物质中化学键的数目,常见单质、化合物中所含共价键的种类和数目。物质(化学键)CO2(C==O)CH4(C—H)P4(P—P)SiO2(Si—O)石墨(C—C)金刚石(C—C)S8(S—S)Si(Si—Si)每个微粒所含键数(3)活化能与焓变的关系a.催化剂能_______反应的活化能,但不影响焓变的大小。b.在无催化剂的情况,E1为_______的活化能,E2为_______的活化能,ΔH=_________,活化能大小影响反应速率。c.起点、终点能量高低判断反应的ΔH,并且物质的能量越低,物质越_______。4.热化学方程式(1)概念:表示参加反应物质的量和_______的关系的化学方程式。(2)意义:不仅表明了化学反应中的_______变化,也表明了化学反应中的_______变化。例如:H2(g)+O2(g)===H2O(l)ΔH=-285.8kJ·mol-1,表示在25℃和1.01×105Pa下,1molH2(g)和molO2(g)反应生成___________________________________。(3)热化学方程式的书写方法①写出化学方程式并注明各物质的聚集状态。热化学方程式的化学计量数表示的是____________,可以是_______或_______。物质的聚集状态:固态用“_______”,液态用“_______”,气体用“_______”,溶液用“_______”。②注明反应时的温度和压强。常用的ΔH的数据,一般都是___________时的数据,可以不特别注明。③用ΔH表示化学反应热,ΔH必须与化学方程式一一对应,注意“+”“-”和单位__________。④ΔH的单位中“mol-1”的含义对一个化学反应,ΔH的单位中“mol-1”不是指每摩尔具体物质,而是指“每摩尔_______”。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应()(2)同温同压下,反应H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同()(3)石墨转变为金刚石是吸热反应,则金刚石比石墨更稳定()(4)800℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,则其热化学方程式为N2(g)+3H2(g)===2NH3(g)ΔH=-38.6kJ·mol-1()(5)所有的燃烧反应都是放热反应,所以不需要加热就能进行()(6)一个反应的焓变因反应物的用量和反应条件的改变而发生改变()(7)可逆...