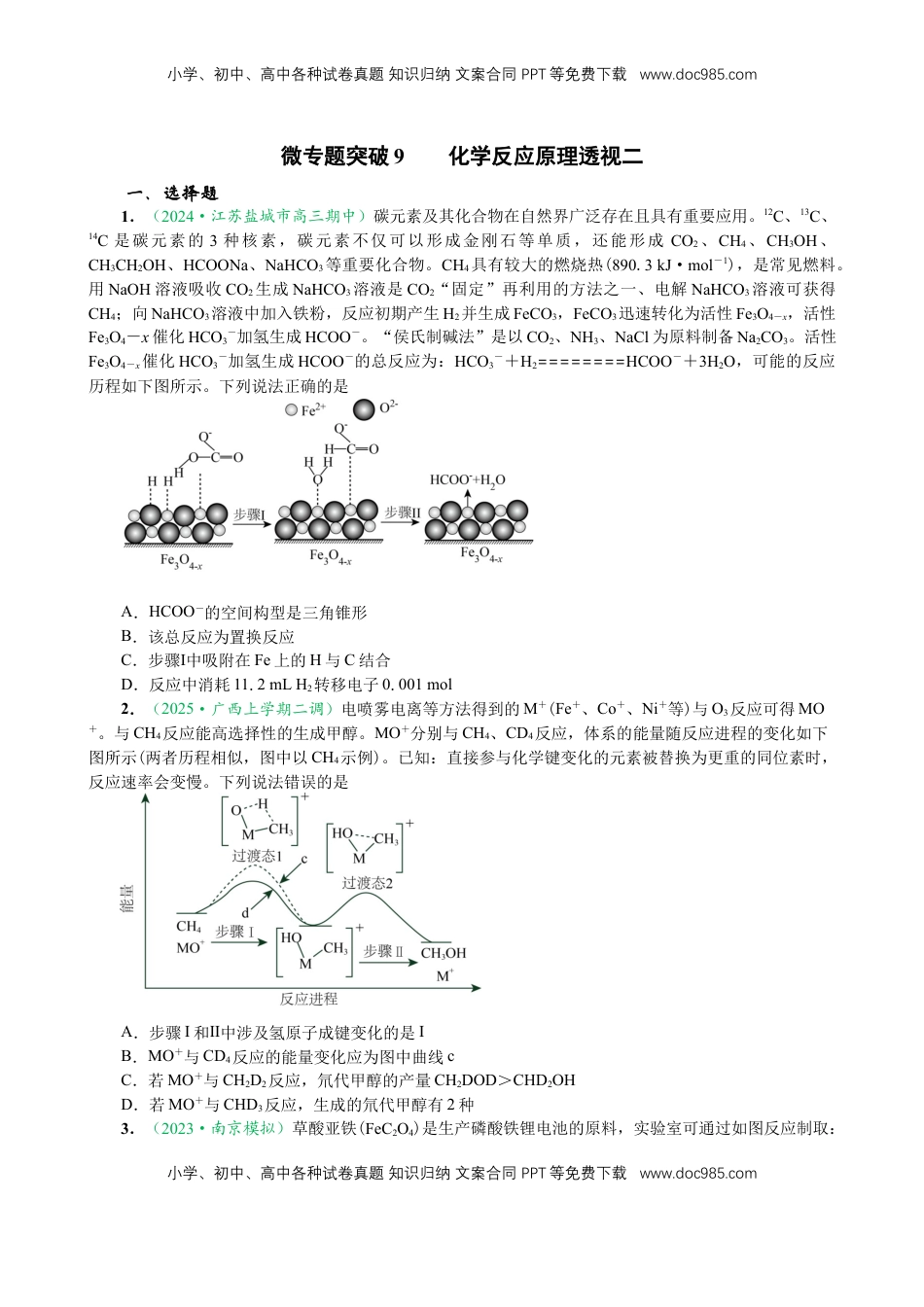
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com微专题突破9化学反应原理透视二一、选择题1.(2024·江苏盐城市高三期中)碳元素及其化合物在自然界广泛存在且具有重要应用。12C、13C、14C是碳元素的3种核素,碳元素不仅可以形成金刚石等单质,还能形成CO2、CH4、CH3OH、CH3CH2OH、HCOONa、NaHCO3等重要化合物。CH4具有较大的燃烧热(890.3kJ·mol-1),是常见燃料。用NaOH溶液吸收CO2生成NaHCO3溶液是CO2“固定”再利用的方法之一、电解NaHCO3溶液可获得CH4;向NaHCO3溶液中加入铁粉,反应初期产生H2并生成FeCO3,FeCO3迅速转化为活性Fe3O4-x,活性Fe3O4-x催化HCO3-加氢生成HCOO-。“侯氏制碱法”是以CO2、NH3、NaCl为原料制备Na2CO3。活性Fe3O4-x催化HCO3-加氢生成HCOO-的总反应为:HCO3-+H2========HCOO-+3H2O,可能的反应历程如下图所示。下列说法正确的是A.HCOO-的空间构型是三角锥形B.该总反应为置换反应C.步骤Ⅰ中吸附在Fe上的H与C结合D.反应中消耗11.2mLH2转移电子0.001mol2.(2025·广西上学期二调)电喷雾电离等方法得到的M+(Fe+、Co+、Ni+等)与O3反应可得MO+。与CH4反应能高选择性的生成甲醇。MO+分别与CH4、CD4反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH4示例)。已知:直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。下列说法错误的是A.步骤I和Ⅱ中涉及氢原子成键变化的是IB.MO+与CD4反应的能量变化应为图中曲线cC.若MO+与CH2D2反应,氘代甲醇的产量CH2DOD>CHD2OHD.若MO+与CHD3反应,生成的氘代甲醇有2种3.(2023·南京模拟)草酸亚铁(FeC2O4)是生产磷酸铁锂电池的原料,实验室可通过如图反应制取:小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com已知室温时:Ka1(H2C2O4)=5.6×10-2、Ka2(H2C2O4)=1.5×10-4、Ksp(FeC2O4)=2.1×10-7。下列说法正确的是A.酸化、溶解后的溶液中存在:2c(Fe2+)+c(H+)<c(NH)+c(OH-)B.室温下,0.10mol·L-1NaHC2O4溶液中存在:c(C2O)<c(H2C2O4)C.向稀硫酸酸化的KMnO4溶液中滴加Na2C2O4溶液至溶液褪色,反应的离子方程式为5C2O+2MnO+8H2O=0CO2↑+2Mn2++16OH-D.室温时反应Fe2++H2C2O4=FeC2O4+2H+的平衡常数K=404.(2023·苏州中学、淮阴中学、姜堰中学、海门中学联考)已知:室温下,Ka1(H2S)=10-7,Ka2(H2S)=10-12.9。通过下列实验探究含硫化合物的性质。实验1:测得0.1mol·L-1NaHS溶液的pH>7。实验2:向0.1mol·L-1NaHS溶液中通入过量Cl2,无淡黄色沉淀产生。实验3:向0.1mol·L-1NaHS溶液中加入等体积0.1mol·L-1NaHCO3溶液充分混合,无气泡产生。下列说法正确的是A.由实验1可知:c(H+)·c(S2-)>c(H2S)·c(OH-)B.实验2说明HS-不能被Cl2氧化C.实验3所得溶液中:c(S2-)+c(HS-)+c(H2S)>c(CO)+c(HCO)+c(H2CO3)D.0.001mol·L-1Na2S溶液中:c(Na+)>c(S2-)>c(OH-)>c(H+)5.(2024·南通海安期末)室温下,通过下列实验探究NaHS溶液的性质。实验实验操作和现象1向0.1mol·L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红2向0.1mol·L-1NaHS溶液中加入等体积0.1mol·L-1NaOH溶液充分混合3向0.1mol·L-1NaHS溶液中通入少量氯气,有淡黄色沉淀产生4向0.1mol·L-1NaHS溶液中加入等体积0.1mol·L-1HCl溶液,有气体放出下列有关说法正确的是A.实验1中0.1mol·L-1NaHS溶液中:c(S2-)>c(H2S)B.实验2中所得溶液中:c(Na+)=c(S2-)+c(HS-)+c(H2S)C.实验3中反应的离子方程式:HS-+Cl2=S↓+H++2Cl-D.实验4中所得溶液中:c(S2-)+c(OH-)=c(H2S)+c(H+)6.(2023·泰州期末)室温下,某兴趣小组通过下列实验制备少量NaHCO3并探究其性质。实验1:测得100mL14mol·L-1氨水的pH约为12。实验2:向上述氨水中加NaCl粉末至饱和,通入足量CO2后析出晶体。实验3:将所得混合物静置后过...