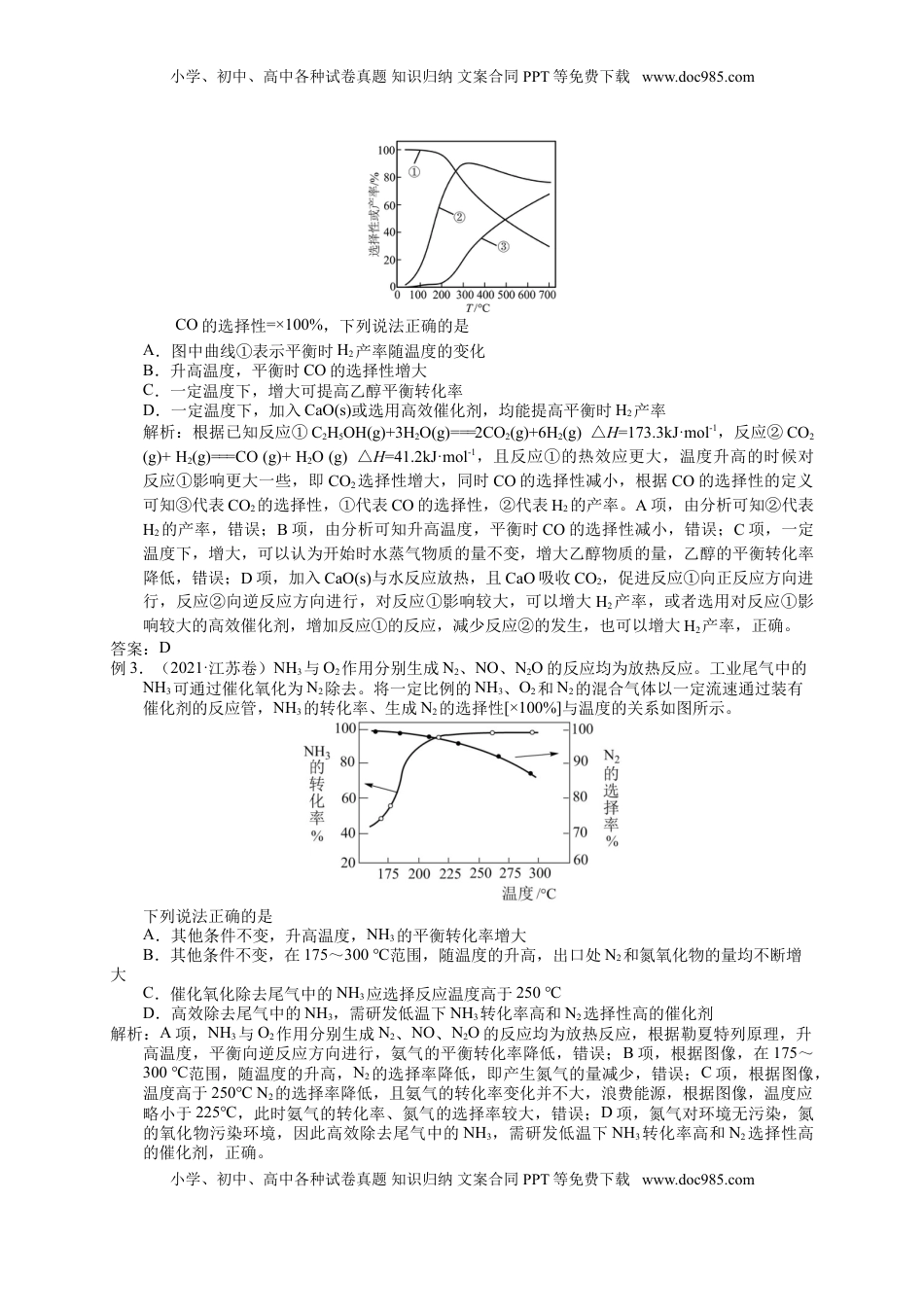
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com2025届高三化学一轮专题复习讲义(12)专题三基本理论3-5化学平衡(二)(1课时,共2课时)【复习目标】1.了解化学平衡常数(K)的含义,能利用化学平衡常数进行相关计算。2.理解外界条件(浓度、温度、压强、催化剂等)对化学平衡的影响,能用相关理论解释其一般规律。3.了解化学平衡的调控在生活、生产和科学研究领域中的重要作用【重点突破】1.能运用平衡移动原理,解决生活中的相关问题,讨论化学反应条件的选择和优化。综合考虑化学反应速率、原料利用率、设备要求、催化剂的活性等,控制合适的反应条件。2.联想外界条件的改变对化学反应速率和化学平衡的影响规律,根据图像中表现的关系与所学规律相对比,做出符合题目要求的判断。能充分考查学生读图、提取信息、解决问题的能力。【真题再现】例1.(2023·江苏卷)二氧化碳加氢制甲烷过程中的主要反应为CO2(g)+4H2(g)===CH4(g)+2H2O(g)△H=-164.7kJ·mol-1CO2(g)+H2(g)===CO(g)+H2O(g)△H=41.2kJ·mol-l在密闭容器中,1.01×10-5Pa、n起始(CO2)︰n起始(H2)=1︰4时,CO2平衡转化率、在催化剂作用下反应相同时间所测得的CO2实际转化率随温度的变化如题13图所示。CH4的选择性可表示为×100%。下列说法正确的是A.反应2CO(g)+2H2(g)===CO2(g)+CH4(g)的熔变△H=-205.9kJ·mol-1B.CH4的平衡选择性随着温度的升高而增加C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃D.450℃时,提高的值或增大压强,均能使CO2平衡转化率达到X点的值解析:A项,由盖斯定律可知反应2CO(g)+2H2(g)===CO2(g)+CH4(g)的焓变△H=-2×41.2kJ·mol-1-164.7kJ·mol-1=-247.1kJ·mol-1,错误;B项,CO2(g)+4H2(g)===CH4(g)+2H2O(g)为放热反应,升高温度平衡逆向移动,CH4的含量降低,故CH4的平衡选择性随着温度的升高而降低,错误;C项,由图可知,已知条件之下,该催化剂催化二氧化碳反应温度范围约为380℃时二氧化碳转化率最大,此时为最适温度,温度继续增加,催化剂活性下降,错误;D项,450℃时,提高的值可提高二氧化碳的平衡转化率,增大压强反应I平衡正向移动,可提高二氧化碳的平衡转化率,均能使CO2平衡转化率达到X点的值,D正确。答案:D例2.(2022·江苏卷)乙醇-水催化重整可获得H2。其主要反应为C2H5OH(g)+3H2O(g)===2CO2(g)+6H2(g)△H=173.3kJ·mol-1CO2(g)+H2(g)===CO(g)+H2O(g)△H=41.2kJ·mol-1在1.0×105Pa、n始(C2H5OH)∶n始(H2O)=1∶3时,若仅考虑上述反应,平衡时CO2和CO的选择性及H2的产率随温度的变化如图所示。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comCO的选择性=×100%,下列说法正确的是A.图中曲线①表示平衡时H2产率随温度的变化B.升高温度,平衡时CO的选择性增大C.一定温度下,增大可提高乙醇平衡转化率D.一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时H2产率解析:根据已知反应①C2H5OH(g)+3H2O(g)===2CO2(g)+6H2(g)△H=173.3kJ·mol-1,反应②CO2(g)+H2(g)===CO(g)+H2O(g)△H=41.2kJ·mol-1,且反应①的热效应更大,温度升高的时候对反应①影响更大一些,即CO2选择性增大,同时CO的选择性减小,根据CO的选择性的定义可知③代表CO2的选择性,①代表CO的选择性,②代表H2的产率。A项,由分析可知②代表H2的产率,错误;B项,由分析可知升高温度,平衡时CO的选择性减小,错误;C项,一定温度下,增大,可以认为开始时水蒸气物质的量不变,增大乙醇物质的量,乙醇的平衡转化率降低,错误;D项,加入CaO(s)与水反应放热,且CaO吸收CO2,促进反应①向正反应方向进行,反应②向逆反应方向进行,对反应①影响较大,可以增大H2产率,或者选用对反应①影响较大的高效催化剂,增加反应①的反应,减少反应②的发生,也可以增大H2产率,正确。答案:D例3.(2021·江苏卷)NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业尾气中的NH3可通过催化氧化为N2除去。将一定比例的NH3、O2和N2的混合气体以一定流速通...