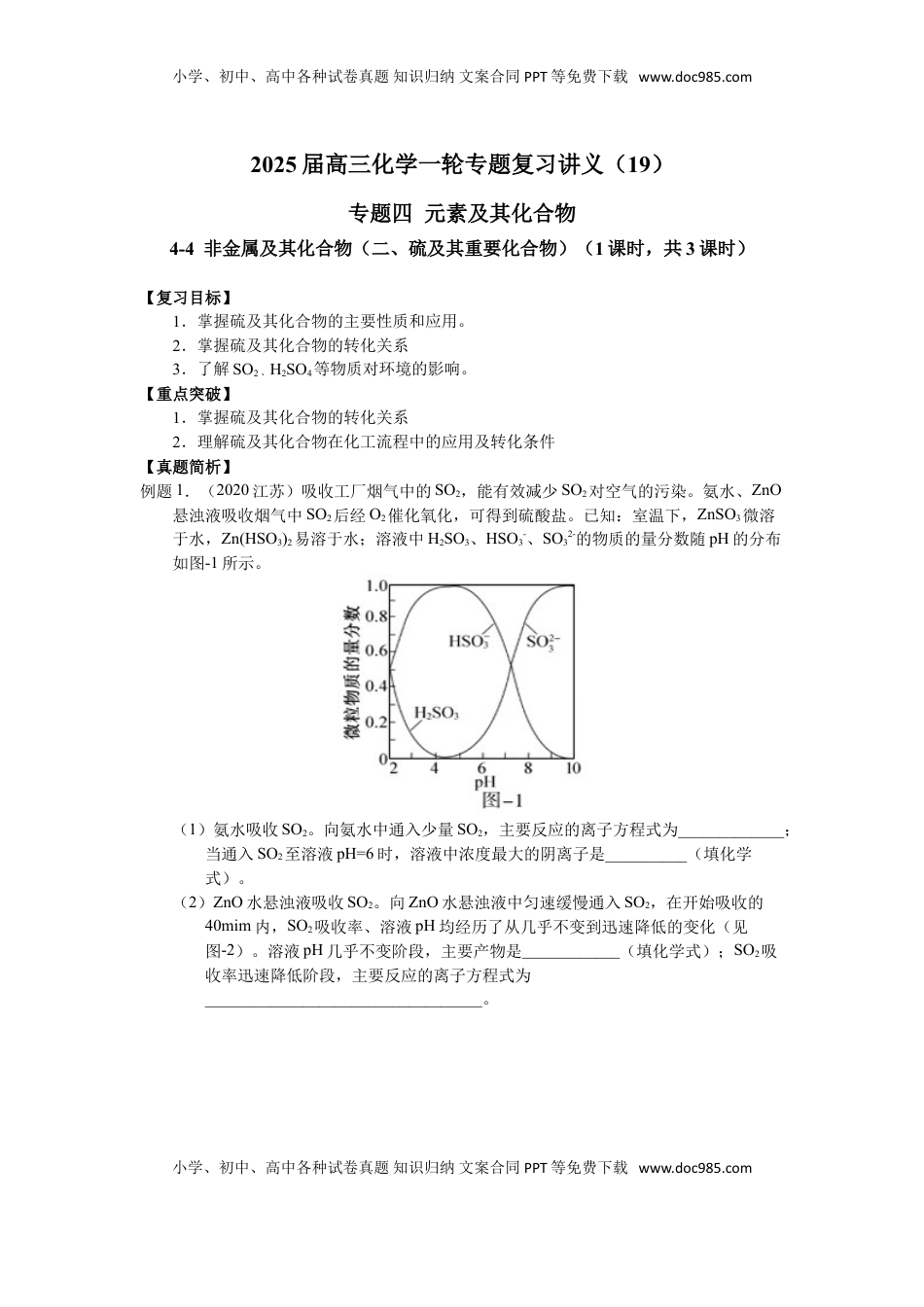
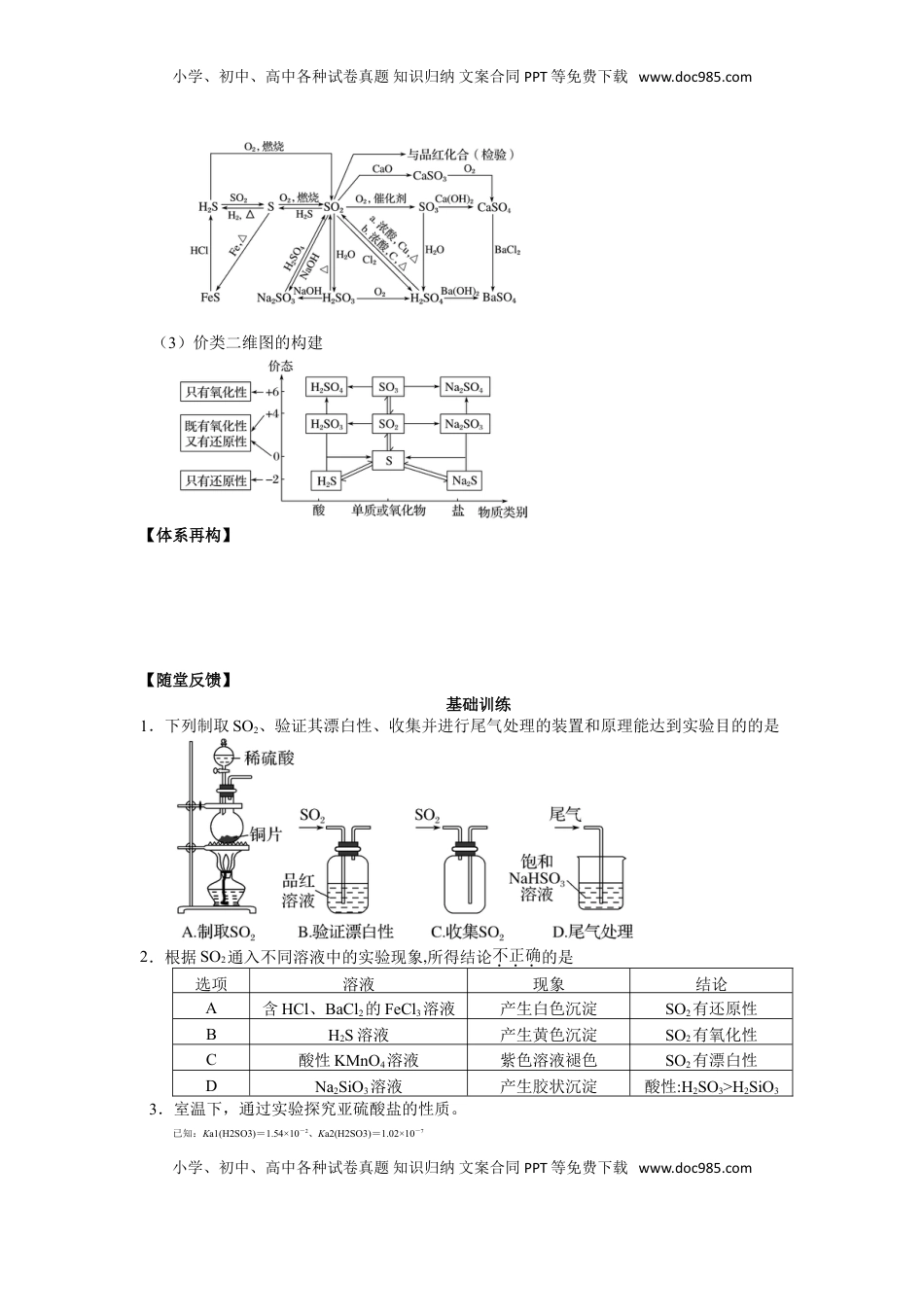
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com2025届高三化学一轮专题复习讲义(19)专题四元素及其化合物4-4非金属及其化合物(二、硫及其重要化合物)(1课时,共3课时)【复习目标】1.掌握硫及其化合物的主要性质和应用。2.掌握硫及其化合物的转化关系3.了解SO2、H2SO4等物质对环境的影响。【重点突破】1.掌握硫及其化合物的转化关系2.理解硫及其化合物在化工流程中的应用及转化条件【真题简析】例题1.(2020江苏)吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为_____________;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是__________(填化学式)。(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40mim内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是____________(填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为__________________________________。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO42-生成速率越大,其主要原因是____________;随着氧化的进行,溶液的pH将__________(填“增大”、“减小”或“不变”)。解析:(1)向氨水中通入少量SO2时,SO2与氨水反应生成亚硫酸铵,反应的离子方程式为2NH3+H2O+SO2=2NH4++SO32-(或2NH3·H2O+SO2=2NH4++SO32-+H2O);根据图-1所示,pH=6时,溶液中不含有亚硫酸,仅含有HSO3-和SO32-,根据微粒物质的量分数曲线可以看出溶液中阴离子浓度最大的是HSO3-;(2)反应开始时,悬浊液中的ZnO大量吸收SO2,生成微溶于水的ZnSO3,此时溶液pH几乎不变;一旦ZnO完全反应生成ZnSO3后,ZnSO3继续吸收SO2生成易溶于水的Zn(HSO3)2,此时溶液pH逐渐变小,SO2的吸收率逐渐降低,这一过程的离子方程式为ZnSO3+SO2+H2O=Zn2++2HSO3-(或ZnO+2SO2+H2O=Zn2++2HSO3-)(3)pH值大于6.5时,SO2以微溶物ZnSO3形式存在,使SO2不利于与O2接触,反应速率慢;pH降低,SO2主要以HSO3-形式溶于水中,与O2充分接触。因而pH降低,SO42-生成速率增大;随着反应的不断进行,大量的HSO3-反应生成SO42-,反应的离子方程式为2HSO3-+O2=2SO42-+2H+,随着反应的不断进行,有大量的氢离子生成,导致氢离子浓度增大,溶液pH减小。答案:(1)2NH3+H2O+SO2===2NH4++SO32-或2NH3·H2O+SO2===2NH4++SO32-+H2OHSO3-(2)ZnSO3ZnSO3+SO2+H2O===Zn2++2HSO3-或ZnO+2SO2+H2O===Zn2++2HSO3-(3)随着pH降低,HSO浓度增大减小小结:向氨水中通入少量的SO2,反应生成亚硫酸铵,结合图像分析pH=6时溶液中浓度最大的阴离子;通过分析ZnO吸收SO2后产物的溶解性判断吸收率变化的原因;通过分析HSO3-与氧气反应的生成物,分析溶液pH的变化情况。【知识整合】(1)理清知识主线H2S→S→SO2→SO3(H2SO4)(2)形成网络构建小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com(3)价类二维图的构建【体系再构】【随堂反馈】基础训练1.下列制取SO2、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是2.根据SO2通入不同溶液中的实验现象,所得结论不正确的是选项溶液现象结论A含HCl、BaCl2的FeCl3溶液产生白色沉淀SO2有还原性BH2S溶液产生黄色沉淀SO2有氧化性C酸性KMnO4溶液紫色溶液褪色SO2有漂白性DNa2SiO3溶液产生胶状沉淀酸性:H2SO3>H2SiO33.室温下,通过实验探究亚硫酸盐的性质。已知:Ka1(H2SO3)=1.54×10-2、Ka2(H2SO3)=1.02×10-7小学、初中、高中各种试卷真题知识归纳文案合同PP...