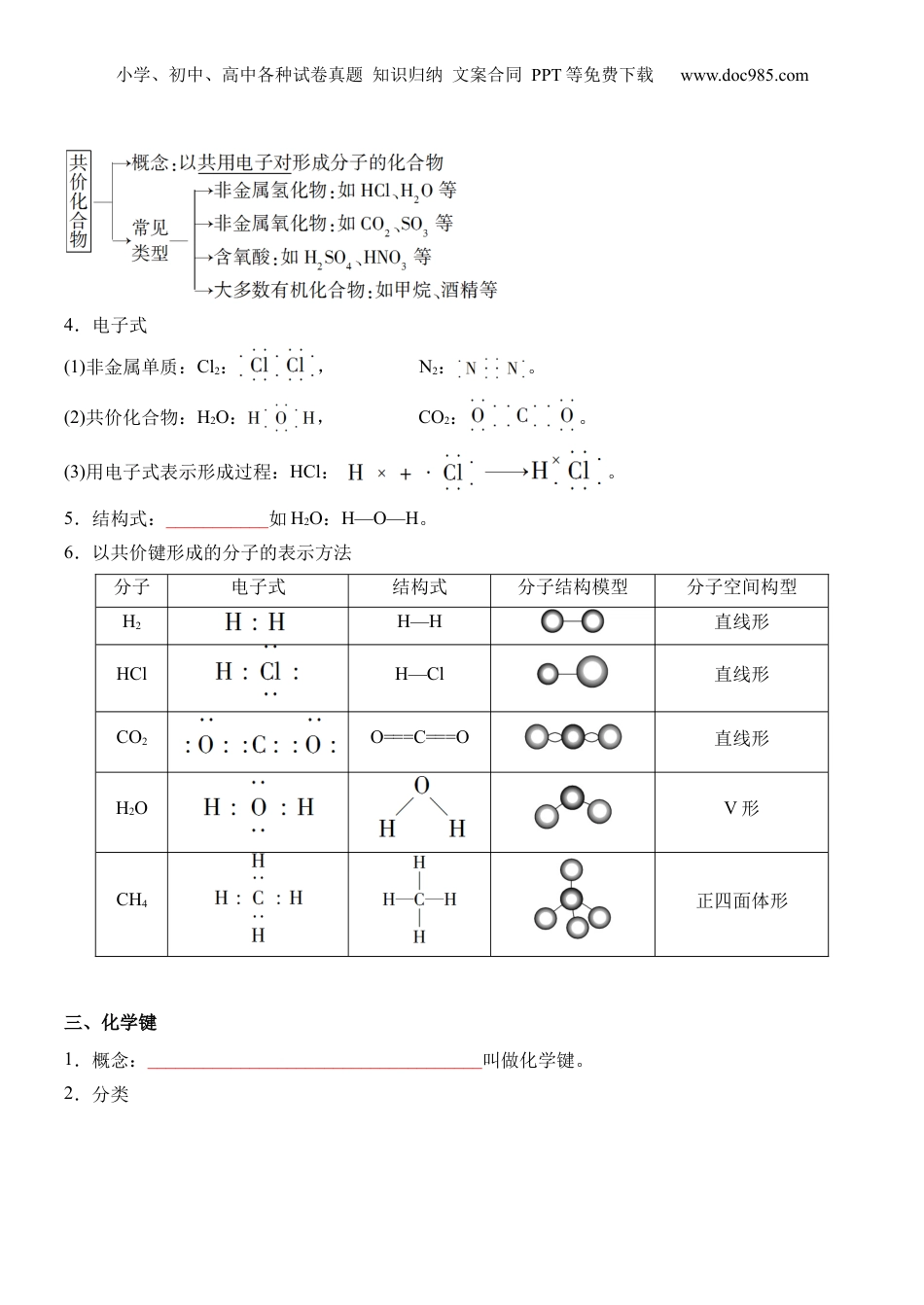
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com第18讲化学键1.了解离子键的概念及形成过程。2.了解离子化合物的概念,并能识别常见的离子化合物。3.掌握原子、阴阳离子及离子化合物电子式的书写方法,并会用电子式表示离子化合物的形成过程4.了解共价键的概念及形成过程,了解极性键和非极性键的区别。5.掌握共价分子电子式和结构式的书写方法,会用电子式表示共价分子的形成过程。6.了解化学键的含义,能从化学键的角度理解化学反应的实质。一、离子键和离子化合物1.NaCl的形成示意图:钠离子和氯离子通过___________在一起,形成氯化钠。2.离子键:___________叫做离子键。成键粒子:___________。成键元素:___________。【易错点拨】离子键的本质是___________的静电作用,既包括静电吸引也包括静电排斥。3.离子化合物:小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com4.电子式:___________式子。粒子电子式的表示方法粒子电子式的表示方法(举例)原子离子阳离子阴离子化合物用电子式表示离子化合物的形成过程。如NaCl:。二、共价键和共价化合物1.共价键形成过程(以Cl2的形成为例):定义:____________________________________________。成键粒子:___________。成键元素:____________________________________________。2.分类3.共价化合物小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com4.电子式(1)非金属单质:Cl2:,N2:。(2)共价化合物:H2O:,CO2:。(3)用电子式表示形成过程:HCl:。5.结构式:___________如H2O:H—O—H。6.以共价键形成的分子的表示方法分子电子式结构式分子结构模型分子空间构型H2H—H直线形HClH—Cl直线形CO2O===C===O直线形H2OV形CH4正四面体形三、化学键1.概念:____________________________________叫做化学键。2.分类小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【判断物质中所含化学键类型的思路】(1)首先___________。只含有共价键的物质有非金属单质(稀有气体除外)、非金属氧化物、酸、大部分有机物;只含有离子键的物质有大多数金属氧化物、简单的盐(如NaCl)、金属氢化物等;既含共价键又含离子键的物质有碱、含复杂离子的盐(如NH4Cl)、含活泼金属的特殊化合物(如Na2O2)。(2)其次___________。非金属元素原子之间一般形成共价键,活泼金属与活泼非金属元素原子之间一般形成离子键。(3)化学反应的过程,___________,二者缺一不可。有化学键断裂或形成的过程不一定发生化学变化。例如:①离子化合物的熔化过程。离子化合物熔化后电离成自由移动的阴、阳离子,离子键被破坏,只发生了物理变化。②电解质的溶解过程。电解质溶于水后,形成自由移动的阴、阳离子,化学键断裂,只发生了物理变化。3.化学反应的本质(1)表象:__________________________。(2)本质:_________________________。四、分子间作用力1.定义:_______________________________________________,最初叫范德华力。2.规律:一般说来,____________________________________,分子间作用力越大,物质的熔、沸点也就越高,如卤素单质的熔、沸点:F2<Cl2<Br2<I2。3.氢键:如液态NH3、H2O和HF中分子之间存在的一种比分子间作用力稍强的相互作用,叫氢键,氢键不是化学键,___________。(1)氢键的形成条件:①___________,即氢原子处在X—H···Y之间。②氢只有跟非金属性强的并且其原子半径小的元素化合后,才能形成较强的氢键,这样的元素有N、O、F等。(2)___________:①氢键对物质熔、沸点的影响:分子间形成的氢键会使物质的熔点和沸点升高,这是因为固体熔化或液体汽化时必须破坏分子间的氨键,从而需要消耗更多的能量。②分子间形成氢键对___________等也有影响。如NH3极易溶于水,主要是因为氨分子与水分子之间易形成氢键。③水中氢键对水的密度也有影响,水结成冰时体积膨胀,密度减小,主要是小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com_________________________________________...