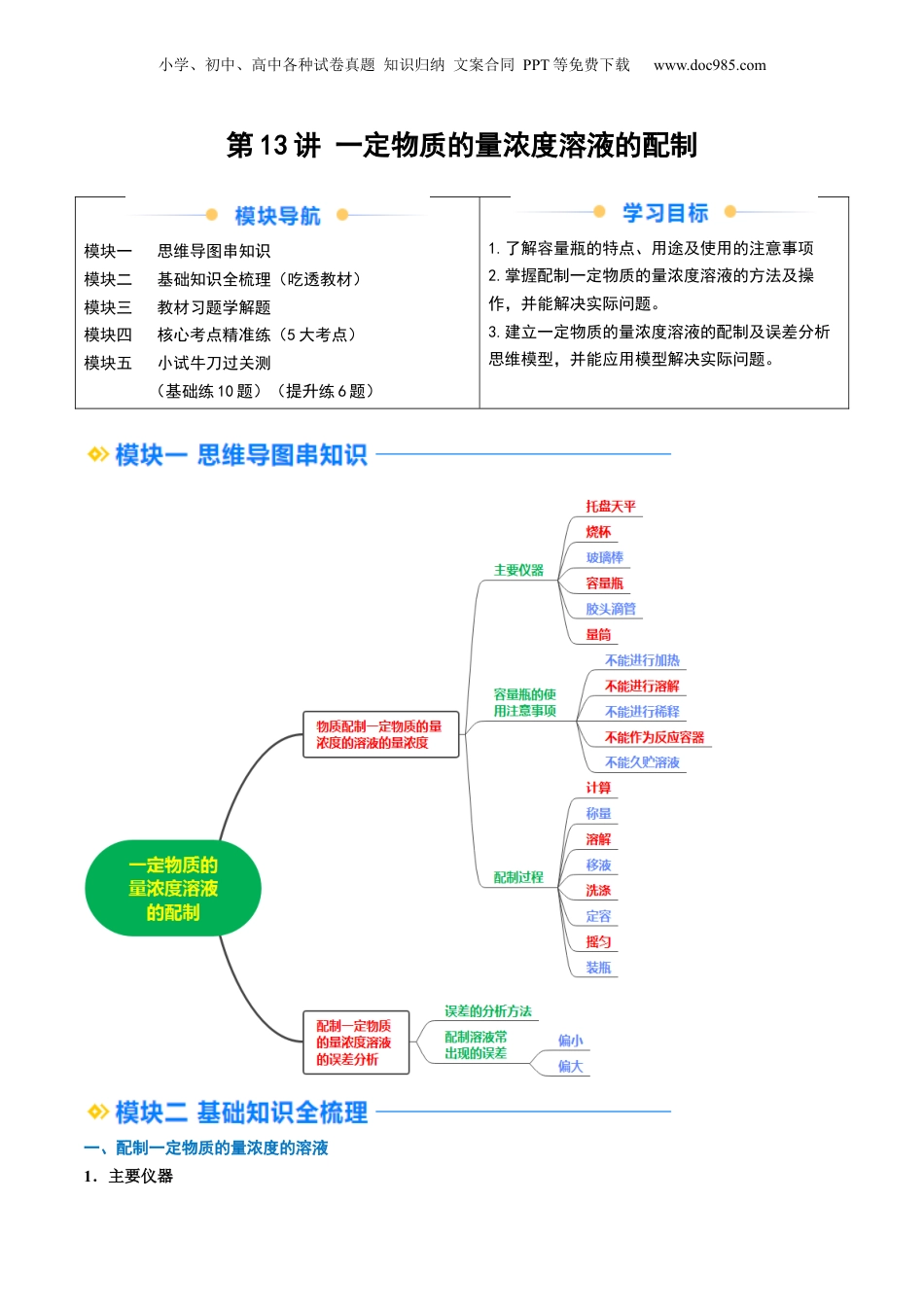
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com第13讲一定物质的量浓度溶液的配制模块一思维导图串知识模块二基础知识全梳理(吃透教材)模块三教材习题学解题模块四核心考点精准练(5大考点)模块五小试牛刀过关测(基础练10题)(提升练6题)1.了解容量瓶的特点、用途及使用的注意事项2.掌握配制一定物质的量浓度溶液的方法及操作,并能解决实际问题。3.建立一定物质的量浓度溶液的配制及误差分析思维模型,并能应用模型解决实际问题。一、配制一定物质的量浓度的溶液1.主要仪器小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com托盘天平(分析天平)、烧杯、、、、。2.容量瓶的使用注意事项(1)使用前用洗净。(2)用玻璃棒时,玻璃棒与容量瓶的接触点应在刻度线以下。(3)时要平视刻度线,使凹液面最低点与刻度线相切。(4)在容量瓶上标有一个刻度,两个数据(温度和体积)。在选择容量瓶时,应选用与所配溶液体积相等或规格的容量瓶。(5)使用容量瓶的“五不”:不能进行;不能进行;不能进行;不能作为;不能久贮溶液,尤其是碱液。3.配制过程以配制100mL1.00mol·L-1的氯化钠溶液为例思考与交流:能否将固体或液体直接在容量瓶中溶解或稀释,并解释原因。【归纳总结】(1)容量瓶是配制一定物质的量浓度溶液的专用仪器,选择容量瓶应遵循“大而近”的原则,即所配溶液的体积等于或略小于容量瓶的容积。(2)使用容量瓶注意“五不”:不能溶解固体;不能稀释浓溶液;不能加热;不能作反应容器;不能长期贮小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com存溶液。二、配制一定物质的量浓度溶液的误差分析1.误差的分析方法在分析配制一定物质的量浓度溶液的误差时,要根据cB==来分析,其中MB(溶质的摩尔质量)为定值。(1)V不变,凡是使mB或nB增大(或减小)的操作均使cB偏大(或偏小)。(2)nB或mB不变,凡是使V增大(或减小)的操作均使cB偏小(或偏大)。2.配制100mL1.00mol·L-1的氯化钠溶液常出现的误差能引起误差的操作因变量cnV称量①砝码生锈(没有脱落)②少量氯化钠粘在称量纸上③使用游码,且药品砝码位置颠倒移液④有少量液体溅出⑤容量瓶内有少量水⑥未洗涤或洗涤液未注入容量瓶定容⑦仰视刻度线超过刻度线,吸出一部分水⑧摇匀后液面下降,补充水⑨装瓶试剂瓶刚用蒸馏水洗过⑩【特别提醒】溶液配制过程中出现误差一般需要重新配制。【易错警示】俯视、仰视导致的误差分析(1)用容量瓶定容:(影响溶液的体积)①图:定容时俯视刻度线,溶液体积偏小,所配制溶液的浓度偏高。Ⅰ②图:定容时仰视刻度线,溶液体积偏大,所配制溶液的浓度偏低。Ⅱ(2)用量筒量取一定体积的溶液:(影响溶质的物质的量)①图:若俯视刻度线,则实际量取的液体体积偏小,所配溶液浓度偏低。Ⅲ②图:若仰视刻度线,则实际量取的液体体积偏大,所配溶液浓度偏高。Ⅳ教材习题01解题思路小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com关于容量瓶的几种叙述:①是配制一定物质的量浓度的溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水;⑤需要240mL一定物质的量浓度的氯化钠溶液,用250mL的容量瓶配制;⑥用蒸馏水洗净后,再用待配溶液润洗。这些叙述正确的是()A.①②③④⑤B.②③⑤⑥C.①②④⑥D.②③④⑥教材习题02某学生欲配制0.1mol·L-1氢氧化钠溶液100mL,下列操作会造成实际浓度偏高的是()A.空盘时天平指针指向左边B.把烧碱放在滤纸上称量C.定容时俯视刻度线D.使用部分变质的烧碱解题思路核心考点一:配制一定物质的量浓度的仪器【例1】用36.5%的浓盐酸(ρ=1.2g·cm-3)配制1mol·L-1的稀盐酸100mL,配制过程需要用到哪些仪器,且先后顺序正确的是()①100mL量筒②10mL量筒③50mL烧杯④托盘天平⑤100mL容量瓶⑥胶头滴管⑦玻璃棒A.①⑥③⑤⑥⑦B.②⑥③⑦⑤⑥C.③⑤⑦⑥①D.④③⑦⑤⑥核心考点二:配制一定物质的量浓度的溶液的操作【例2】配制500mL0.1mol·L-1的NaCl溶液,下列说法或操作正确的是()A.准确称量2.9gNaCl固体溶于500mL蒸馏水B....