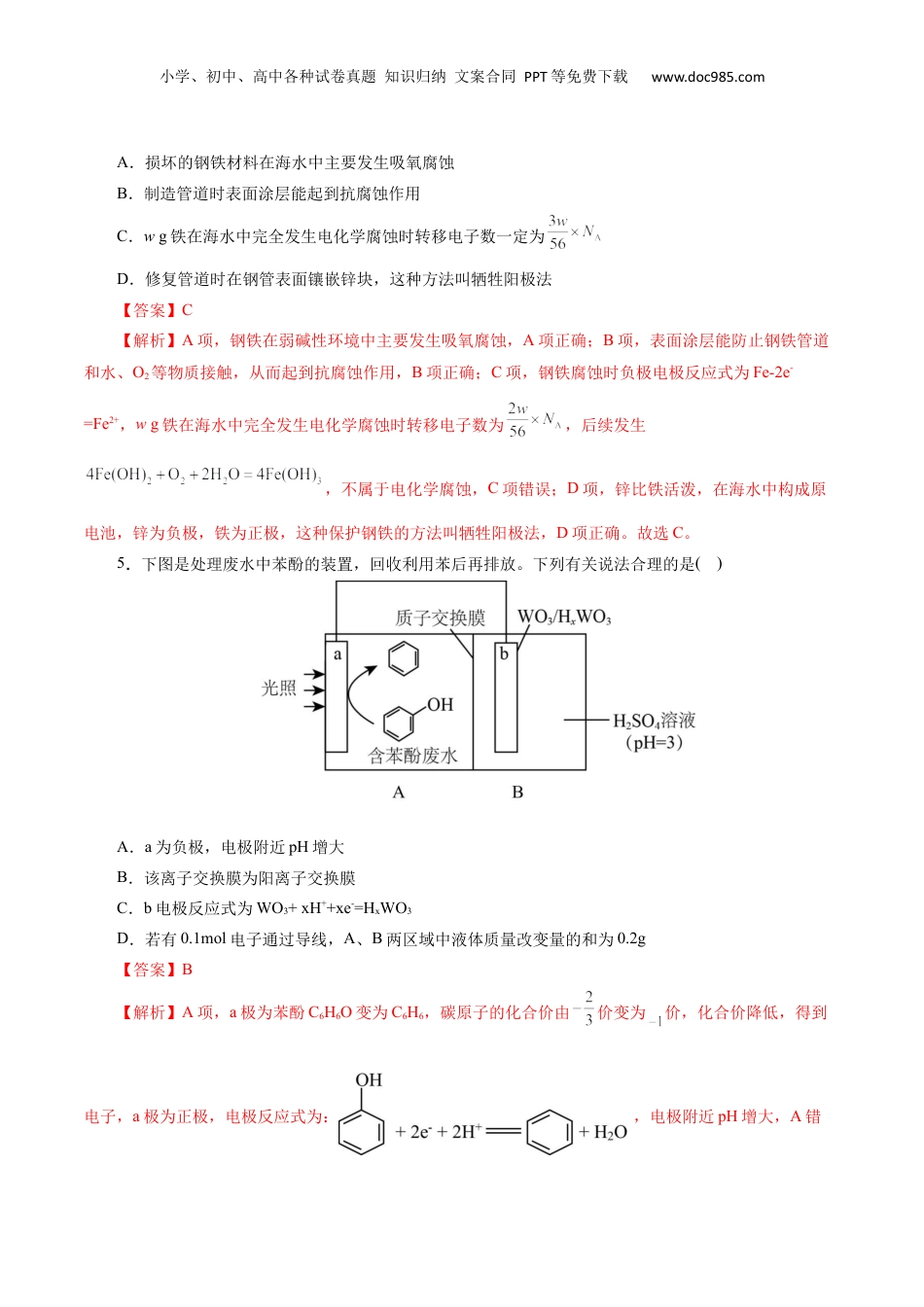
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com专题05化学反应与能量(考试时间:75分钟试卷满分:100分)一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)1.某化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,则下列说法中正确的是()A.该反应为放热反应,无需加热就可以发生B.断裂1molA-A键和1molB-B键要吸收xkJ的能量C.根据图示可知生成1molAB(g)放出的能量D.三种物质A2(g)、B2(g)、AB(g)中,最稳定的物质一定是AB(g)【答案】B【解析】A项,由图可知反应物总能量高于生成物能量为放热反应,但A-A键和B-B键断裂需要吸收能量,可能需要加热破坏反应物化学键以发生反应,反应放热与反应是否需要加热无关,选项A错误;B项,断裂1moLA-A键和1molB-B键要吸收xkJ的能量,选项B正确;C项,根据图示可知生成1molAB(g)放出的能量,选项C错误;D项,物质能量越低越稳定,由图知A2(g)和B2(g)的总能量高于2AB(g)的能量,但不知单独物质的能量大小,所以无法确定谁最稳定,选项D错误;故选B。2.(2024·江苏无锡高三教学质量调研测试)1mol液态肼完全燃烧生成N2气体和液态水放出577kJ的热量。工业上利用NH3和CO2制取尿素[CO(NH2)2],尿素在高温条件下可将汽车尾气中的NOx转化为无毒气体N2。下列化学反应表示正确的是()A.N2H4燃烧的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(g)ΔH=-577kJ·mol-1B.碱性N2H4燃料电池负极发生的电极反应式:N2H4+4e-+4OH-=N2↑+4H2OC.NaClO氧化氨气制取N2H4的离子方程式:2NH3+ClO-=N2H4+Cl-+H2OD.N2H4与NO2高温下反应的化学方程式:N2H4+NO2N2↑+2H2O【答案】C小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【解析】A项,1mol液态肼完全燃烧生成N2气体和液态水放出577kJ的热量,则N2H4燃烧的热化学方程式为:N2H4(l)+O2(g)=N2(g)+2H2O(l)ΔH=-577kJ·mol-1,故A错误;B项,负极失电子,负极反应为:N2H4-4e-+4OH-=N2↑+4H2O,故B错误;C项,NaClO氧化氨气制取N2H4,1molNaClO得2mol电子,1mol氨气失1mol电子,根据得失电子守恒得离子方程式:2NH3+ClO-=N2H4+Cl-+H2O,故C正确;D项,1molN2H4失去4mol电子生成氮气,1mol二氧化氮得4mol电子生成氮气,根据得失电子守恒得反应方程式:2N2H4+2NO23N2↑+4H2O,故D错误;故选C。3.(2024·河北迁安市高三期中)下列装置能达到实验目的是()A.用图Ⅰ所示装置测定55mL1mol/L盐酸与50mL11mol/LNaOH溶液发生中和反应的反应热B.为探究铁制品生锈,用图Ⅱ所示装置,正极材料是铁C.图Ⅲ所示装置实现Ag+2HCl=2AgC1↓+H2↑D.图Ⅳ装置可实现粗铜的精炼【答案】C【解析】A项,该实验装置没有玻璃搅拌器,碎纸条没有充满这个大烧杯,散热较多,不能用来测定55mL1mol/L盐酸与50mL11mol/LNaOH溶液发生中和反应的反应热,故A错误;B项,为探究铁制品生锈,用图Ⅱ所示装置,正极材料是C,负极材料是Fe,故B错误;C项,图Ⅲ中阳极为Ag电极,电极方程式为:Ag-e-+Cl-=AgCl↓,阴极为C电极,电极方程式为:2H++2e-=H2↑,总反应为:Ag+2HCl=2AgC1↓+H2↑,故C正确;D项,铜的电解精炼装置中粗铜应该为阳极,连接电源的正极,故D错误;故选C。4.(2023·辽宁省名校联盟高考模拟调研卷)“北溪”天然气管道至少泄漏8万吨天然气,近20年间甲烷的温室效应率是CO2的84倍。已知管道接口处有钢铁材料等,海水的pH约为8.0。设NA为阿伏伽德罗常数的值。下列有关叙述不正确的是()小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comA.损坏的钢铁材料在海水中主要发生吸氧腐蚀B.制造管道时表面涂层能起到抗腐蚀作用C.wg铁在海水中完全发生电化学腐蚀时转移电子数一定为D.修复管道时在钢管表面镶嵌锌块,这种方法叫牺牲阳极法【答案】C【解析】A项,钢铁在弱碱性环境中主要发生吸氧腐蚀,A项正确;B项,表面涂层能防止钢铁管道和水、O2等物质接触,从而起到抗腐蚀作用,B项正确;C项,钢铁腐蚀时负极电极反应式为Fe-2e-=Fe2+,wg铁在海水中完全发生电化学腐蚀时转移电子数为,后续发生,不属于电化学腐蚀,C项错误;D项,...