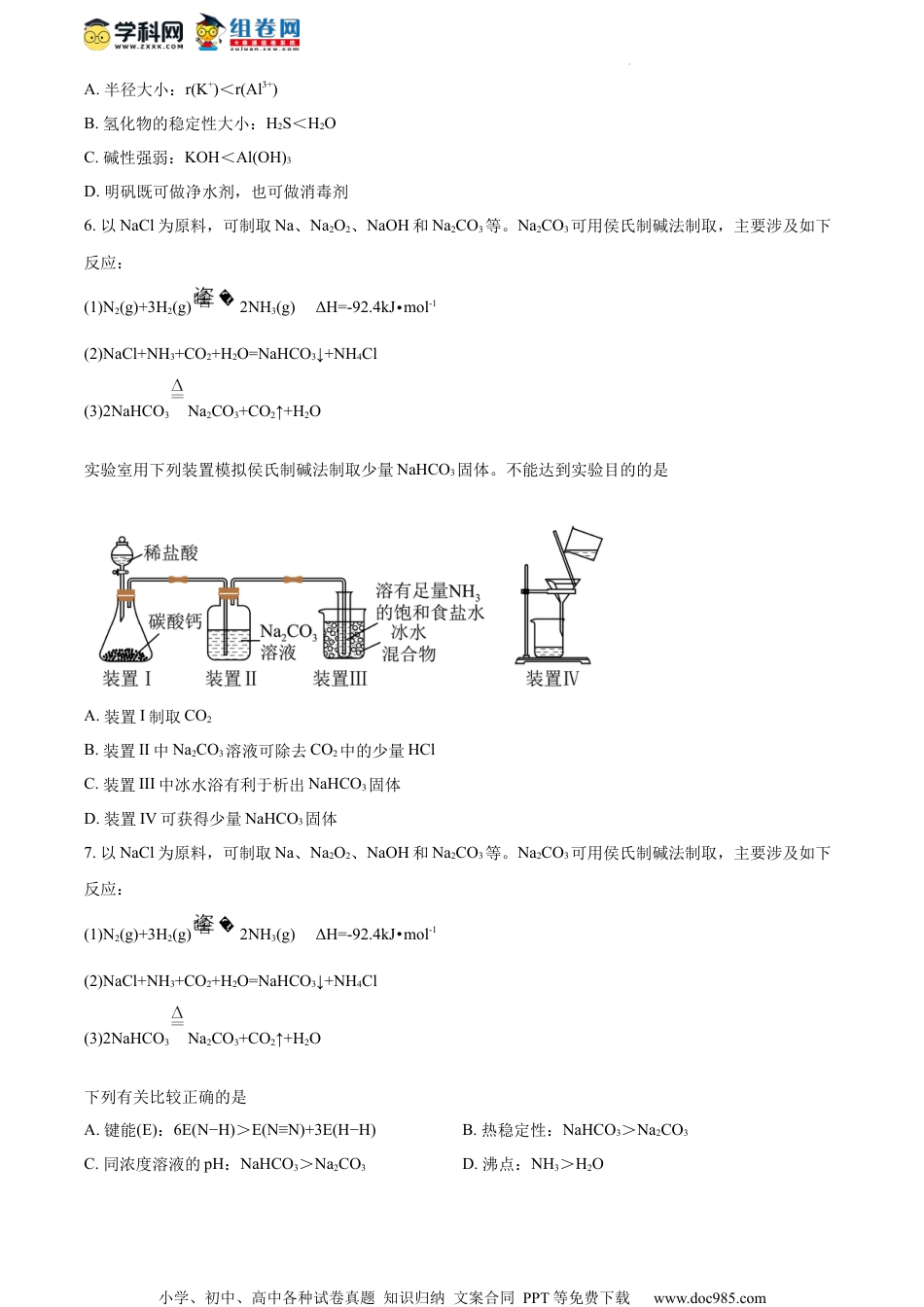
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com2022-2023学年第一学期八校高三年级联合调研化学试卷可能用到的相对原子质量:H-1C-12N-14O-16Na-23Al-27S-32K-39Ca-40Mn-55Fe-56I-127Ce-140第I卷一、选择题:本大题共13小题,共39分,每题只有一个选项符合题意。1.2022年北京冬奥会上的火炬“飞扬”、定制款滑雪板、碲化镉发电玻璃,以及全气候电池等无不散发着化学高科技的魅力。下列有关说法不正确的是A.火炬中的燃料氢气燃烧时释放热量B.普通玻璃可用碳酸钠等来制造C.由碲和镉合成碲化镉时碲作氧化剂D.电动汽车充电时化学能转化为电能2.从烟道气分离回收硫的基本反应:。下列说法正确的是A.该反应属于置换反应B.铝土矿的主要成分为C.在该反应中表现出氧化性D.、CO和均属于酸性氧化物3.少量Na2O2与H2O反应生成H2O2和NaOH。下列说法正确的是A.Na2O2的电子式为B.H2O电离方程式为:H2O=H++OH-C.H2O2中O元素的化合价为-1D.NaOH仅含离子键4.下列有关物质的性质与用途具有对应关系的是A.NaCl易溶于水,可用于工业电解制备钠B.FeCl3溶液具有酸性,可用于腐蚀印刷电路板上的CuC.次氯酸(盐)具有不稳定性,可作杀菌消毒剂,还可作漂白剂D.氨气具有还原性,用浓氨水检验氯气管道是否泄漏5.明矾[KAl(SO4)2•12H2O]可用于净水。下列说法正确的是小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comA.半径大小:r(K+)<r(Al3+)B.氢化物的稳定性大小:H2S<H2OC.碱性强弱:KOH<Al(OH)3D.明矾既可做净水剂,也可做消毒剂6.以NaCl为原料,可制取Na、Na2O2、NaOH和Na2CO3等。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:(1)N2(g)+3H2(g)2NH3(g)ΔH=-92.4kJ•mol-1(2)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl(3)2NaHCO3Na2CO3+CO2↑+H2O实验室用下列装置模拟侯氏制碱法制取少量NaHCO3固体。不能达到实验目的的是A.装置I制取CO2B.装置II中Na2CO3溶液可除去CO2中的少量HClC.装置III中冰水浴有利于析出NaHCO3固体D.装置IV可获得少量NaHCO3固体7.以NaCl为原料,可制取Na、Na2O2、NaOH和Na2CO3等。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:(1)N2(g)+3H2(g)2NH3(g)ΔH=-92.4kJ•mol-1(2)NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl(3)2NaHCO3Na2CO3+CO2↑+H2O下列有关比较正确的是A.键能(E):6E(N−H)>E(N≡N)+3E(H−H)B.热稳定性:NaHCO3>Na2CO3C.同浓度溶液的pH:NaHCO3>Na2CO3D.沸点:NH3>H2O小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com8.以NaCl为原料,可制取Na、Na2O2、NaOH和Na2CO3等。Na2CO3,可用侯氏制碱法制取,主要涉及如下反应:N2(g)+3H2(g)2NH3(g)ΔH=-92.4kJ·mol-1NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl2NaHCO3Na2CO3+CO2↑+H2O对于反应N2(g)+3H2(g)2NH3(g),下列说法正确的是A.该反应的ΔS>0B.该反应的平衡常数可表示为C.其他条件相同,增大,H2转化率减小D.使用催化剂能降低该反应的焓变9.工业上制备下列物质的生产流程不合理的是A.由黄铁矿制硫酸:B.由重晶石制可溶性钡盐:重晶石C.由石英砂制高纯硅:石英砂D.由铝土矿冶炼铝:铝土矿10.室温下,下列各组离子在指定溶液中能大量共存的是A.能使甲基橙变红的溶液中:Cu2+、Na+、CH3COO-、NOB.0.1mol•L-1KMnO4溶液:NH、Na+、NO、I-C.0.1mol•L-1K2CO3溶液:Na+、Ba2+、Cl-、OH-D.=10-12的溶液中:Mg2+、Al3+、NO、SO11.下列反应中的离子方程式书写正确的是小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comA.用石墨作电极电解NaCl溶液:2Cl-+2H+Cl2↑+H2↑B.向FeI2溶液中通入少量Cl2:2I-+Cl2=I2+2Cl-C.0.1mol/LNa2CO3溶液pH>7:CO+H2O=H2CO3+2OH-D.向CaCO3中滴加稀醋酸,产生气体:CaCO3+2H+=Ca2++CO2↑+H2O12.室温下,下列实验探究方案及现象能达到探究目的的是选项探究方案及现象探究目的A用pH计测量醋酸、盐酸的pH,比较溶液pH大小醋酸是弱电解质B向久置的溶液中加入足量溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解不能被空气氧化C向NaBr溶液中滴加过量氯水,溶液变橙色,再加入淀粉KI溶液,溶液变蓝色氧化性:D向盛有溶液...